题目内容
《化学反应原理》
在密闭容器中的可逆反应CO(g)+NO2(g)?CO2(g)+NO(g)达到平衡后,
(1)增大压强,则化学反应速率 (填“增大”或“减小”),化学平衡 (填“向正反应方向”“向逆反应方向”或“不”)移动.
(2)容器容积不变,升高温度后,气体的颜色明显加深.则该可逆反应的正方向为 (填“吸热”或“放热”)反应.
(3)该反应的化学平衡常数表达式:K= .
在密闭容器中的可逆反应CO(g)+NO2(g)?CO2(g)+NO(g)达到平衡后,
(1)增大压强,则化学反应速率
(2)容器容积不变,升高温度后,气体的颜色明显加深.则该可逆反应的正方向为
(3)该反应的化学平衡常数表达式:K=
考点:化学平衡的影响因素,化学平衡常数的含义
专题:化学平衡专题
分析:(1)压强增大,反应速率加快,化学平衡向着气体系数和减小的方向进行;
(2)升高温度,化学平衡向着吸热方向进行;
(3)化学平衡常数K=
.
(2)升高温度,化学平衡向着吸热方向进行;
(3)化学平衡常数K=
| 各生成物平衡浓度系数次幂之积 |
| 各个反应物平衡浓度系数次方的积 |
解答:
解:(1)压强增大,反应CO(g)+NO2(g)?CO2(g)+NO(g)的反应速率加快,化学平衡向着气体系数和减小的方向进行,但是该反应前后气体系数和不变,所以平衡不移动,故答案为:增大;不;
(2)升高温度,化学平衡CO(g)+NO2(g)?CO2(g)+NO(g)向着吸热方向进行,气体的颜色明显加深,所以二氧化氮浓度增大,反应逆向进行,该反应是放热的,故答案为:放热;
(3)化学平衡常数K=
=
,故答案为:
.
(2)升高温度,化学平衡CO(g)+NO2(g)?CO2(g)+NO(g)向着吸热方向进行,气体的颜色明显加深,所以二氧化氮浓度增大,反应逆向进行,该反应是放热的,故答案为:放热;
(3)化学平衡常数K=
| 各生成物平衡浓度系数次幂之积 |
| 各个反应物平衡浓度系数次方的积 |
| c(CO2)?c(NO) |
| c(CO)?c(NO2) |
| c(CO2)?c(NO) |
| c(CO)?c(NO2) |
点评:该题考查学生化学平衡移动原理的应用以及化学平衡常数的表达式书写知识,难度不大.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
实验是化学研究的基础,图中所示的实验方法、装置或操作正确的是( )
A、 除杂质 |
B、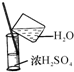 稀释 |
C、 制气 制气 |
D、 称量 |
下列化合物中,既能由单质直接化合制得,又能由复分解反应制得的是( )
| A、CuS |
| B、FeS |
| C、Al2S3 |
| D、FeCl2 |
某些液体用肉眼难以区分是胶体还是溶液.区分胶体和溶液的实验方法可行的是( )
| A、一束光照射 | B、加热至沸 |
| C、静置沉降 | D、过滤 |

 Ⅰ.已知:温度过高时,WO2(s)转变为WO2(g):
Ⅰ.已知:温度过高时,WO2(s)转变为WO2(g):