题目内容
10.下列物质属于混合物的是( )| A. | 纯碱 | B. | 小苏打 | C. | 烧碱 | D. | 赤铁矿 |
分析 纯净物是指相同物质组成的物质,混合物是不同物质组成的物质,纯碱为碳酸钠、小苏打为碳酸氢钠、烧碱为氢氧化钠都属于化合物,赤铁矿的主要成分为氧化铁为混合物.
解答 解:A.纯碱是碳酸钠,是一种物质组成的纯净物,故A不符合;
B.小苏打是碳酸氢钠,是一种物质组成的纯净物,故B不符合
C.烧碱是氢氧化钠,是一种物质组成的纯净物,故C不符合
D.赤铁矿是由氧化铁等多种物质组成的混合物,故D符合;
故选D.
点评 本题考查了物质分类的方法,物质俗称和成分的分析判断,掌握概念实质是解题关键,题目较简单.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
18.配制100mL 0.1mol/L的NaCl溶液,下列操作会导致所配溶液浓度偏高的是( )
| A. | 称量时,左盘高,右盘低 | B. | 定容时,俯视读取刻度 | ||
| C. | 容量瓶洗净后未干燥 | D. | 定容时,液面超过了刻度线 |
5.下列表述正确的是( )
| A. | SO3和NxOy都属于酸性氧化物 | |
| B. | 实验室制取氯气时,先加热二氧化锰,后滴入浓盐酸 | |
| C. | 锶与镁、钙、钡同族,由于碳酸钙和碳酸钡都难溶,所以碳酸锶也难溶 | |
| D. | 结构和组成相似的物质,沸点随相对分子质量增大而升高,所以NH3沸点低于PH3 |
15.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | 含有大量AlO${\;}_{2}^{-}$的溶液中:Na+、OH-、Cl-、CO${\;}_{3}^{2-}$ | |
| B. | 滴加紫色石蕊试液变红的溶液中:K+、Ba2+、CH3COO-、F- | |
| C. | 加入Al能放出H2的溶液中:K+、NH4+、NO3-、HCO3- | |
| D. | 1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
2.下列离子方程式书写正确的( )
| A. | Na2CO3溶液中通入少量SO2:SO2+H2O+2CO32-═SO32-+2HCO3- | |
| B. | 漂白粉中滴加浓盐酸加热制取氯气:ClO-+Cl-+2H+ $\frac{\underline{\;\;△\;\;}}{\;}$ Cl2+H2O | |
| C. | 将0.1mol•L-1的NH4Al(SO4)2溶液与0.2mol•L-1的Ba(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═AlO2-↓+2BaSO4↓+2H2O | |
| D. | 含0.4molFeI2的溶液中通入0.3mol氯气:4Fe2++2I-+3Cl2═4Fe3++I2+6Cl- |
20. X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:
X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:
(1)Y在元素周期表中的位置是第三周期ⅢA族.
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是O2- (填离子符号).
(3)Q和R按原子个数比1:1组成的化合物甲,是一种“绿色”氧化剂.
①甲的电子式是 .
.
②空气阴极法电解制备甲的装置如图所示.在碱性溶液中,将空气中的氧气还原得到甲和稀碱的溶液,则图中直流电源的a是正极.
 X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:
X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是O2- (填离子符号).
(3)Q和R按原子个数比1:1组成的化合物甲,是一种“绿色”氧化剂.
①甲的电子式是
 .
.②空气阴极法电解制备甲的装置如图所示.在碱性溶液中,将空气中的氧气还原得到甲和稀碱的溶液,则图中直流电源的a是正极.

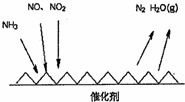 随着我国工业化水平的不断发展,解决水、空气污染问题成为重要课题.
随着我国工业化水平的不断发展,解决水、空气污染问题成为重要课题.