题目内容
7.内锌矿的主要成分为ZnS,含有杂质PbS、CuS、FeS、SiO2等,以闪锌矿制备氯化锌的流程如图所示.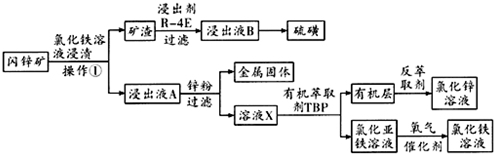
请回答下列问题:
(1)配制氯化铁浸渍液时要求pH为0.8~1之间,pH太高则铁离子会水解,pH太低,浸渍矿石会产生有害气体硫化氢,操作①是过滤.由氯化锌溶液制备氯化锌晶体的方法是加入盐酸再蒸发.
(2)高沸点溶剂R-4E几乎不溶于水,120℃时硫在R-4E里的溶解度为365g,室温时溶解度为35.9g,从浸出液B提取硫的方法是冷却饱和溶液.硫是工业制备硫酸的原料,现有1吨矿石,硫的总含量为24%,最多制备浓度98%的硫酸0.75吨.
(3)氯化铁与硫化锌发生反应:2FeCl3+ZnS═ZnCl2+2FeCl2+S,则氯化铁与FeS反应的方程式为2FeCl3+FeS═3FeCl2+S.
(4)溶液X的成分的化学式为ZnCl2、FeCl2,该流程中循环使用的物质是溶剂R-4E、有机萃取剂TBP、氯化铁溶液.
(5)由氯化亚铁溶液制备氯化铁溶液,可以用H2O2、Cl2,但生产成本高.酸性条件下,使用催化剂在50℃左右通入氧气转化的成本极低,反应的离子方程式为4Fe2++4H++O2$\frac{\underline{催化剂}}{△}$4Fe3++2H2O.
分析 依据流程分析,闪锌矿的主要成分为ZnS,含有杂质PbS、CuS、FeS、SiO2等,用氯化铁溶液浸取,发生氧化还原反应生成硫单质,过滤得矿渣中含有硫、二氧化硅等,滤液A中含有氯化亚铁、氯化锌、氯化铅等,矿渣用高沸点溶剂R-4E浸取出硫,经过冷却结晶可得硫单质,溶剂R-4E可循环利用,滤液A中加入锌,置换出溶液中的铜离子、亚铅离子等,过滤除去置换出的金属,得氯化锌、氯化亚铁的混合溶液X,溶液X中加入有机萃取剂TBP,将有机层再反萃取,得氯化锌溶液,有机萃取剂TBP可循环利用,氯化亚铁溶液中通入氯气得氯化铁溶液,氯化铁溶液可循环利用,据此答题.
解答 解:(1)因为铁离子会水解呈酸性,所以配制氯化铁浸渍液时要求pH为0.8~1之间,防止铁离子水解,矿石的主要成份为硫化物,溶液pH太低,会产生硫化氢气体,分离固体和液体一般用过滤操作,由氯化锌溶液制备氯化锌晶体时,要防止锌离子水解产生氢氧化锌,所以操作的方法是加入盐酸再蒸发,
故答案为:铁离子会水解;硫化氢;过滤;加入盐酸再蒸发;
(2)根据题中数据,硫在R-4E里的溶解度受温度影响较大,所以从浸出液B提取硫的方法是冷却饱和溶液,1吨矿石,硫的总含量为24%,所以硫元素的质量为0.24t,根据硫元素守恒可知,可制备浓度98%的硫酸的质量为$\frac{0.24}{32×98%}×98$t=0.75t,
故答案为:冷却饱和溶液;0.75;
(3)根据氯化铁与硫化锌发生反应:2FeCl3+ZnS═ZnCl2+2FeCl2+S可知,氯化铁与FeS反应,铁离子能氧化-2价的硫生成硫单质,反应的方程式为2FeCl3+FeS═3FeCl2+S,
故答案为:2FeCl3+FeS═3FeCl2+S;
(4)根据上面的分析可知,溶液X的成分的化学式为ZnCl2、FeCl2,该流程中循环使用的物质是溶剂R-4E、有机萃取剂TBP、氯化铁溶液,
故答案为:ZnCl2、FeCl2;溶剂R-4E、有机萃取剂TBP、氯化铁溶液;
(5)酸性条件下,使用催化剂在50℃左右通入氧气可将亚铁离子氧化成铁离子,反应的离子方程式为4Fe2++4H++O2$\frac{\underline{催化剂}}{△}$4Fe3++2H2O,
故答案为:4Fe2++4H++O2$\frac{\underline{催化剂}}{△}$4Fe3++2H2O.
点评 本题为工艺流程题,通过氯化锌的制备,考查了盐类的水解、化学方程式、离子方程式的书写、物质分离提纯的方法等,明确工艺流程及各种物质的性质是解题关键,题目难度中等.

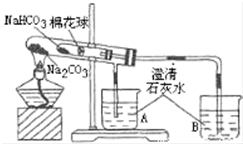 某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,如表是他们撰写的实验报告的一部分.
某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,如表是他们撰写的实验报告的一部分. | 实验序号 | 实验步骤(内容) | 现象 |
| ① | 在贴有标签a、b的试管中分别加入1.0gNa2CO3固体和NaHCO3固体,观察外观. | / |
| ② | 继续向两试管中分别加入10.0mL水,用力振荡,观察现象. | / |
| ③ | 再分别向两试管中滴加2滴酚酞溶液,观察现象. | 溶液变红 |
| ④ | 加热大试管一段时间.(注:棉花球沾有无水硫酸铜粉末) | 有无水硫酸铜粉末的棉花球变蓝,A烧杯中没有明显现象,B烧杯中有白色沉淀生成 |
(2)已知:20℃时Na2CO3的溶解度为20.5g.由实验②(填实验序号)现象可知,20℃时NaHCO3的溶解度小于20.5g;如果向饱和Na2CO3溶液中不断通入CO2气体,现象是白色晶体析出,化学方程式是Na2CO3+CO2+H2O=2NaHCO3↓.
(3)由实验④可以得出结论是碳酸钠的稳定性强于碳酸氢钠,用化学方程式说明得出结论的原因2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
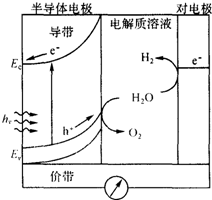 太阳能发电和阳光分解水制氢气,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面.如图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带是未充填电子的能级最低的能带,半导体价带是已充填价电子的能级最高的能带,图中的e-为电子、h+为空穴.在光照下,电子(e-)由价带跃迁到导带后,然后流向对电极.下列说法不正确的是( )
太阳能发电和阳光分解水制氢气,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面.如图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带是未充填电子的能级最低的能带,半导体价带是已充填价电子的能级最高的能带,图中的e-为电子、h+为空穴.在光照下,电子(e-)由价带跃迁到导带后,然后流向对电极.下列说法不正确的是( )| A. | 对电极表面发生的电极反应式为:4H++4e-→2H2 | |
| B. | 电池的总反应式为:2H2O$\stackrel{hv}{→}$O2+2H2↑ | |
| C. | 整个过程中实现了太阳能向电能化学能等的转化 | |
| D. | 装置中电流的方向是从半导体电极流向对电极 |
 、NO3-、SO42- D.H+、Na+、HCO3-、NO3-
、NO3-、SO42- D.H+、Na+、HCO3-、NO3-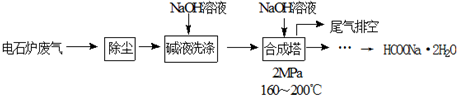
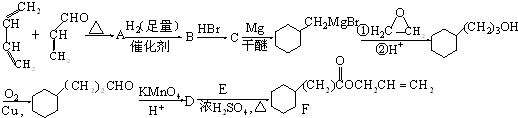
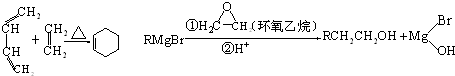
 ,A中所含官能团的名称是醛基、碳碳双键.
,A中所含官能团的名称是醛基、碳碳双键. .
. .
.