题目内容
下列电子式正确的是( )
A、H2O2 |
B、MgCl2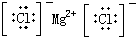 |
C、NaOH  |
D、CCl4 |
考点:电子式
专题:化学用语专题
分析:A.H2O2分子中不存在阴阳离子,不能标出电荷;
B.MgCl2是离子化合物,根据离子化合物的电子式书写方法判断;
C.氢氧化钠为离子化合物,要加括号和电荷;
D.CCl4中Cl原子周围8个电子.
B.MgCl2是离子化合物,根据离子化合物的电子式书写方法判断;
C.氢氧化钠为离子化合物,要加括号和电荷;
D.CCl4中Cl原子周围8个电子.
解答:
解:A.H2O2属于共价化合物,不存在离子键,分子中氢原子与氯原子之间形成共用电子对,其电子式为: ,故A错误;
,故A错误;
B.MgCl2为离子化合物,2个氯离子位于镁离子两边,氯化镁的电子式为: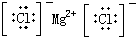 ,故B正确;
,故B正确;
C.氢氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,NaOH的电子式: ,故C错误;
,故C错误;
D.CCl4为共价化合物,各原子满足8电子稳定结构,电子式为 ,故D错误,
,故D错误,
故选B.
 ,故A错误;
,故A错误; B.MgCl2为离子化合物,2个氯离子位于镁离子两边,氯化镁的电子式为:
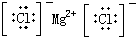 ,故B正确;
,故B正确;C.氢氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,NaOH的电子式:
 ,故C错误;
,故C错误;D.CCl4为共价化合物,各原子满足8电子稳定结构,电子式为
 ,故D错误,
,故D错误,故选B.
点评:本题考查电子式的判断,难度不大,要明确用电子式表示离子化合物、共价化合物、阴离子及单质分子的方法.

练习册系列答案
相关题目
把4.6g钠放入200mL 0.1mol/L的AlCl3溶液中,待其充分反应后,下列叙述中错误的是( )
| A、Cl-的浓度几乎不变 |
| B、溶液呈浑浊 |
| C、溶液中几乎不存在Al3+ |
| D、溶液中存在最多的离子是Na+ |
火法炼铜首先要焙烧黄铜矿,其反应为2CuFeS2+O2=Cu2S+2FeS+SO2.下列说法不正确的是( )
| A、SO2既是氧化产物又是还原产物 |
| B、CuFeS2仅作还原剂,硫元素被氧化 |
| C、每转移0.8mol电子,有0.2mol硫被氧化 |
| D、每生成1mol Cu2S,有1mol硫被氧化 |
受热到一定程度就能软化的高聚物主要是( )
| A、相对分子质量较大的高聚物 |
| B、分子结构复杂的高聚物 |
| C、体型结构的高聚物 |
| D、线型结构的高聚物 |
同位素Si中发现新的物理学“幻数”,下列有关
Si的说法不正确的是( )
42 14 |
A、
| ||
B、
| ||
C、
| ||
D、
|
海水提镁的主要流程如下:

下列说法正确的是( )
①试剂M是盐酸
②流程中的反应全部都是非氧化还原反应
③操作b只是过滤
④用海水晒盐后的饱和溶液加石灰乳制Mg(OH)2
⑤电解熔融MgCl2比电解熔融的MgO制金属镁更节约能量.

下列说法正确的是( )
①试剂M是盐酸
②流程中的反应全部都是非氧化还原反应
③操作b只是过滤
④用海水晒盐后的饱和溶液加石灰乳制Mg(OH)2
⑤电解熔融MgCl2比电解熔融的MgO制金属镁更节约能量.
| A、①②③④⑤ | B、②③ |
| C、④⑤ | D、①④⑤ |
某无色溶液中,可大量共存的离子组是( )
| A、Na+、HCO3-、SO42-、Cl- |
| B、Cu2+、NO3-、Cl-、SO42- |
| C、H+、Cl-、Na+、CO32- |
| D、K+、Mg2+、SO42-、OH- |
三种短周期元素A、B、C,它们的原子序数依次递增,它们的原子的最外层电子数之和为10.A与C在周期表中同主族,B原子最外层电子数等于A原子次外层电子数.下列叙述正确的是( )
| A、原子半径A<B<C |
| B、单质B在一定条件下可以通过置换反应得到单质A |
| C、C的氧化物的熔点比A的氧化物的低 |
| D、A与C可形成离子化合物 |