题目内容
下列各组中的离子,能在溶液中大量共存的是( )
| A、Cu2+、Ba2+、C1-、SO42- |
| B、K+、Na+、OH-、C1- |
| C、Na+、H+、SO42-、OH- |
| D、H+、Na+、Cl-、CO32- |
考点:离子共存问题
专题:离子反应专题
分析:离子之间不反应生成气体、沉淀、弱电解质或发生氧化还原反应、双水解反应的就能共存,据此分析解答.
解答:
解:A.Ba2+、SO42-反应生成硫酸钡白色沉淀,所以不能共存,故A错误;
B.这几种离子之间不反应,所以能大量共存,故B正确;
C.H+、OH-反应生成弱电解质水,所以不能大量共存,故C错误;
D.H+、CO32-反应生成二氧化碳和水,所以不能大量共存,故D错误;
故选B.
B.这几种离子之间不反应,所以能大量共存,故B正确;
C.H+、OH-反应生成弱电解质水,所以不能大量共存,故C错误;
D.H+、CO32-反应生成二氧化碳和水,所以不能大量共存,故D错误;
故选B.
点评:本题考查离子共存,为高考高频点,明确离子性质及离子共存条件是解本题关键,还常常与盐类水解、氧化还原反应、离子颜色、溶液pH等联合考查.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
下列有机物中,属于高分子化合物的是( )
| A、油脂 | B、蔗糖 |
| C、葡萄糖 | D、蛋白质 |
下列中的实验一定不会出现沉淀现象的是( )
| A、CO2气体通入NaAlO2溶液中 |
| B、SO2气体通入BaCl2溶液中 |
| C、CO2气体通入饱和Na2CO3溶液中 |
| D、SO2气体通入Ba(OH)2溶液中 |
工业上向锅炉里注入Na2CO3.溶液浸泡,将水垢中的CaSO4转化为CaCO3而后用盐酸去除.下列叙述不正确的是( )
| A、温度升高.Na2CO3溶液的Kw和c(OH一)均会增大 |
| B、沉淀转化的离子方程式为CO32-十CaSO4=CaCO3+SO42- |
| C、盐酸溶液中,CaCO3的溶解性大于CaSO4 |
| D、Na2CO3溶液遇CO2后,阴离子浓度均减小 |
与水一样,甲醇也能微弱电离:2CH3OH(l)═CH3OH2++CH3O-,25℃时,K=2.0×10-17.若往一定量的甲醇中加入金属钠,则有关叙述正确的是( )
| A、金属钠与甲醇反应比金属钠与水反应更剧烈 |
| B、结合H+的能力CH3O->OH- |
| C、所得到溶液中K=c(CH3O-)×c(CH3OH2+) |
| D、所得到溶液中c(Na+)=c(CH3OH2+)+c(CH3O-) |
下列晶体模型对应的物质熔化时破坏共价键的是( )
A、 金刚石模型 金刚石模型 |
B、 干冰模型 |
C、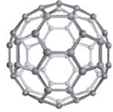 碳60模型 |
D、 氯化钠模型 |
下列说法正确的是( )
| A、SO3溶于水后能导电,故SO3为电解质 |
| B、强电解质的水溶液中不存在大量溶质分子 |
| C、向NaCN溶液中滴入酚酞试液显红色,则HCN为强酸 |
| D、25℃时,用CH3COOH溶液滴定等浓度NaOH溶液至pH=7,V(CH3COOH)<V(NaOH) |