题目内容
7.下列离子方程式不正确的是( )| A. | 将铜片放入稀硫酸中:Cu+2H+═Cu2++H2↑ | |
| B. | 将铁粉放入氯化铜溶液中:Fe+Cu2+═Fe2++Cu | |
| C. | Ba(OH)2溶液中滴入MgCl2溶液中:2OH-+Mg2+═Mg(OH)2↓ | |
| D. | 纯碱中滴加盐酸:CO32-+2H+═H2O+CO2↑ |
分析 A.不符合反应客观事实;
B.二者反应生成氯化亚铁和铜;
C.二者反应生成氢氧化镁和氯化钡;
D.碳酸钠与盐酸反应生成氯化钠、水和二氧化碳.
解答 解:A.铜与稀硫酸不反应,故A错误;
B.将铁粉放入氯化铜溶液中,离子方程式:Fe+Cu2+═Fe2++Cu,故B正确;
C.Ba(OH)2溶液中滴入MgCl2溶液中,离子方程式:2OH-+Mg2+═Mg(OH)2↓,故C正确;
D.纯碱中滴加盐酸,离子方程式:CO32-+2H+═H2O+CO2↑,故D正确;
故选:A.
点评 本题考查了离子方程式的书写,侧重考查复分解反应的离子方程式书写,明确反应实质是解题关键,注意离子反应遵循客观事实,遵循电荷守恒规律,题目难度不大.

练习册系列答案
相关题目
18.一定条件下的密闭容器中:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905.9kJ•mol-1,下列叙述正确的是( )
| A. | 4molNH3和5molO2反应,达到平衡时放出热量为905.9kJ | |
| B. | 平衡时v正(O2)=v逆(NO) | |
| C. | 平衡后降低压强,混合气体平均摩尔质量增大 | |
| D. | 平衡后升高温度,混合气体中NO含量降低 |
19.下列物质在水溶液中的电离方程式书写完全正确的是( )
| A. | KMnO4=K++Mn7++4O2- | B. | Ba(OH)2═Ba2++(OH-)2 | ||
| C. | Mg(NO3)2=Mg+2+2NO3- | D. | NaHCO3═Na++HCO3- |
16.根据如表数据,下列选项正确的是( )
| 化学式 | CH3COOH | H2SO3 | NH3•H2O |
| 电离常数K(25℃) | Ka=1.8×10-5 | Ka1=1.23×10-2;Ka2=6.6×10-8 | Kb=1.8×10-5 |
| A. | Na2SO3溶液中滴加足量醋酸,反应的离子方程式为:SO32-+2CH3COOH=SO2↑+H2O+2CH3COO- | |
| B. | 25℃时,pH=3的醋酸和pH=11的氨水等体积混合后,混合液中水的电离被促进 | |
| C. | NaHSO3溶液呈酸性,是因为Kw/Ka1>Ka2 | |
| D. | 0.1mol/L的CH3COOH溶液与等浓度等体积的CH3COONa混合后,溶液中的微粒存在以下关系:c(H+)+c(CH3COOH)=c(CH3COO-)+c(OH-) |
2.己烷雌酚的一种合成路线如图:

下列叙述不正确的是( )

下列叙述不正确的是( )
| A. | 在NaOH水溶液中加热,化合物X可发生消去反应 | |
| B. | 在一定条件,化合物Y可与HCHO发生缩聚反应 | |
| C. | 用FeCl3溶液可鉴别化合物X和Y | |
| D. | 化合物Y中含有手性碳原子 |
17.如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是( )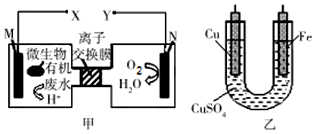

| A. | M电极反应式:(C6H10O5)n+7nH2O-24ne-═6nCO2↑+24nH+ | |
| B. | 铜电极应与X相连接 | |
| C. | 质子透过离子交换膜由右向左移动 | |
| D. | 当N电极消耗0.2 mol气体时,则铁电极增重16g |
14.已知一定温度下合成氨反应:N2+H2═2NH3 (每生成2mol NH3放出92.4kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1mol N2和3mol H2,达平衡时放出热量为Q1,②通入2mol N2和6mol H2,达平衡时放出热量为Q2,则下列关系正确的是( )
| A. | Q2>2 Q1 | B. | Q1=92.4 kJ | C. | Q1<Q2<184.8 kJ | D. | Q1=Q2<92.4 kJ |
 其功能远比我们想象的要大的多,这对硅的纯度要求很高。用化
其功能远比我们想象的要大的多,这对硅的纯度要求很高。用化 学方法可制得高纯度硅,其化学方程式为:①SiO2 + 2C
学方法可制得高纯度硅,其化学方程式为:①SiO2 + 2C  Si + 2CO;②Si + 2Cl2
Si + 2CO;②Si + 2Cl2  SiCl4;③SiCl4 +2H2
SiCl4;③SiCl4 +2H2  Si + 4HCl,其中,反应①和③属于
Si + 4HCl,其中,反应①和③属于