��Ŀ����
14��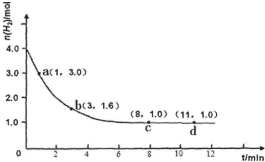 ��ҵ�ϳɰ��ķ�ӦΪ��N2��g��+3H2��g��?2NH3��g����H��0ijʵ�齫3.0mol N2��g����4.0mol H2��g�������ݻ�Ϊ10L���ܱ������У����¶�T1�·�Ӧ�����H2�����ʵ����淴Ӧʱ��ı仯��ͼ��ʾ��
��ҵ�ϳɰ��ķ�ӦΪ��N2��g��+3H2��g��?2NH3��g����H��0ijʵ�齫3.0mol N2��g����4.0mol H2��g�������ݻ�Ϊ10L���ܱ������У����¶�T1�·�Ӧ�����H2�����ʵ����淴Ӧʱ��ı仯��ͼ��ʾ����1����Ӧ��ʼ3min�ڣ�H2��ƽ����Ӧ����Ϊ0.080mol/��L•min����
��2���������ºϳɰ���Ӧ�Ļ�ѧƽ�ⳣ��K=2.0��102 ��L/mol��2���������2λ��Ч���֣�
��3�����ı��¶�ΪT2�� T2С��TI���ٽ���ʵ�飬���ڴ����ͼ�л���H2�����ʵ����淴Ӧʱ��仯��Ԥ�ڽ��ʾ��ͼ��
��4����ij�¶�ʱ��N2��g��+3H2��g��?2NH3��g����K=0.5��
���¶��£���0.5L�ķ�Ӧ�����н��кϳɰ���Ӧ��һ��ʱ����N2��H2��NH3�����ʵ����ֱ�Ϊ2mol��1mol��2mol�����ʱ��Ӧv��N2����=v��N2�����������������������=������ȷ������
��5����֪����ҵ�ϳɰ�ʱ���ϳ�����ÿ����1mol NH3���ų�46.1kJ��������N��N�ļ���Ϊ945.8kJ/mol��H-H�ļ���Ϊ436.0kJ/mol����Ͽ�1mol N-H�������������391kJ
��6������һ��DZ�ڵ������Դ������������ȼ�ϵ�ص�ȼ�ϣ���ص��ܷ�ӦΪ��4NH3��g��+3O2��g���T2N2��g��+6H2O��g�������ȼ�ϵ�صĸ�����Ӧʽ��2NH3-6e-+6OH-=N2+6H2O��
���� ��1������v=$\frac{��c}{��t}$���㷴Ӧ���ʣ�
��2������ƽ��ʱ�����ʵ�Ũ�ȣ�����ƽ�ⳣ������ʽ���㣻
��3����ͼҪ�㣺��T1��T2�������¶ȣ���Ӧ���ʼ�С����λʱ�����������������ʵ�����С���ﵽƽ��ʱ��������������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ��������Ӧ�����ƶ�����ƽ��ʱ���������ʵ�����С��
��4������Qc��K�ô�С��ϵ���жϷ�Ӧ�ķ���
��5���ټ�������2mol�����ų���������ע�����ʵľۼ�״̬�뷴Ӧ����д�Ȼ�ѧ����ʽ��
�ڷ�Ӧ��=��Ӧ���ܼ���-�������ܼ��ܣ�
��6��ԭ��ظ�������������Ӧ�������ڸ���ʧȥ���ӣ��������������ɵ�����ˮ��
��� �⣺��1����Ӧ��ʼ3min�ڣ����������ʵ���1.6mol����v��H2��=$\frac{4.0m-1.6mol}{10L��3min}$=0.080mol/��L•min����
�ʴ�Ϊ��0.080mol/��L•min����
��2����ͼ���֪��ƽ��ʱH2��Ũ��0.10 mol/L����
N2��g��+3H2��g��?2NH3��g��
��ʼŨ�ȣ�mol/L�� 0.30 0.40 0
ת��Ũ�ȣ�mol/L�� 0.10 0.30 0.20
ƽ��Ũ�ȣ�mol/L�� 0.20 0.10 0.20
K=$\frac{0��{2}^{2}}{0.2��0��{1}^{3}}$=2.0��102 ��L/mol��2��
�ʴ�Ϊ��2.0��102 ��L/mol��2��
��3��T1��T2�������¶ȣ���Ӧ���ʼ�С����λʱ�����������������ʵ�����С���ﵽƽ��ʱ��������������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ��������Ӧ�����ƶ�����ƽ��ʱ���������ʵ�����С����ͼ��Ϊ��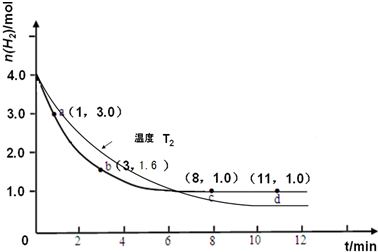 ��
��
�ʴ�Ϊ�� ��
��
��4����0.5L�ķ�Ӧ�����н��кϳɰ���Ӧ��һ��ʱ����N2��H2��NH3�����ʵ����ֱ�Ϊ2mol��1mol��2mol�����ʱ��ӦQc=$\frac{��\frac{2}{0.5}��^{2}}{\frac{2}{0.5}����\frac{1}{0.5}��^{3}}$=0.5=K������
ƽ�ⲻ�ƶ�����v��N2����=v��N2�������ʴ�Ϊ��=��
��5������2mol�����ų�������Ϊ46.1kJ��2=92.2kJ����Ӧ�Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-92.2kJ/mol���ʴ�Ϊ��N2��g��+3H2��g��?2NH3��g����H=-92.2kJ/mol����Ͽ�1mol N-H�������������xkJ����945.8kJ/mol+3��436.0kJ/mol-6��xkJ/mol=-92.2kJ/mol�����x=391��
�ʴ�Ϊ��391��
��6��ԭ��ظ�������������Ӧ�������ڸ���ʧȥ���ӣ��������������ɵ�����ˮ�������缫��ӦʽΪ��2NH3+6OH--6e-=N2+6H2O��
�ʴ�Ϊ��2NH3+6OH--6e-=N2+6H2O��
���� ���⿼�黯ѧƽ�⡢���ʵļ��㡢��Ӧ�ȵļ��㣬��ȷ���η����㼰���ʵ���֮�ȵ������֮�ȵĹ�ϵ���ɽ����Ŀ�ѶȲ���

 �Ƹ�С״Ԫ���ֳ������ϵ�д�
�Ƹ�С״Ԫ���ֳ������ϵ�д� �¸��̵�ѧϵ�д�
�¸��̵�ѧϵ�д� ����ͬѧһ����ʦȫ�źþ�ϵ�д�
����ͬѧһ����ʦȫ�źþ�ϵ�д�2CO2��g��+6H2��g�� CH3CH2OH��g��+3H2O��g����298Kʱ��K1=2.95��1011
2CO��g��+4H2��g�� CH3CH2OH��g��+H2O��g����298Kʱ��K2=1.71��1022
��1��������ͬʱ����Ӧ���뷴Ӧ����ȣ�ת���̶ȸ�����Ǣڣ�
��2����һ��ѹǿ�£���÷�Ӧ�ٵ�ʵ�����������
| �¶ȣ�K�� CO2ת���ʣ�%�� n��H2��/n��CO2�� | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
���¶����ߣ�Kֵ��С���������С�����䡱����
�������̼��[n��H2��/n��CO2��]���������Ҵ������������������������
| A�� | 1 | B�� | 2 | C�� | 6.02��1023 | D�� | 1.204��1024 |
AQIָ����������Ҫ��ȾԴ����ˣ���ȼú����������β��������������̼������ȴ�������ʵ����ɫ���������ܼ��ŵ�Ŀ�ģ�����β��������̼����Ҫԭ��Ϊ��2NO��g��+2CO��g��?N2��g��+2CO��g����H��0��һ�������������崫������ø÷�Ӧ�ڲ�ͬʱ���NO��CO��Ũ�����±�
| ʱ��/s | c��NO��/mol•L-1 | c��CO��/mol•L-1 |
| 0 | 1.00��10-3 | 3.60��10-3 |
| 1 | 4.50��10-4 | 3.05��10-3 |
| 2 | 2.50��10-4 | 2.85��10-3 |
| 3 | 1.50��10-4 | 2.75��10-3 |
| 4 | 1.00��10-4 | 2.70��10-3 |
| 5 | 1.00��10-4 | 2.70��10-3 |
A������ѹǿ B���ϸ��¶�C���Ӵ��� D�������¶�
��2��ǰ2 s�ڵ�ƽ����Ӧ����v��CO2��=3.75��10-4mol/��L•s����COƽ��ת����Ϊ25%
��3���÷�Ӧ��ƽ�ⳣ��KΪ5000
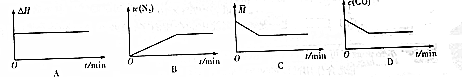
��4���ں����ܱ������г���CO��NO���壬����ͼ����ͼ����ȷ������淴Ӧ�ﵽƽ��״̬����BD
��5������֪
| ��ѧʽ | ���볣�� |
| H2SO3 | K1=1.3��10-2��K2=6.2��10-8 |
| H2CO3 | K1=4.3��10-7��K2=5.6��1011 |
A��HCO3-��HSO3-
B��HCO3-��SO32-
C HCO3-��H2SO3
D��HSO3-��CO32-
�ڵ�������Ũ�ȵ�5����Һ��
a��NH4Cl
b����NH4��2SO4
c����NH4��2CO3
d��NH4Al��SO4��2
e��CH3COONH4��
c��NH4+���ɴ�С��˳����b��c��d��a��e������ĸ��
��6�������ͼװ��ģ������ⶨCO��NO�ķ�Ӧԭ����
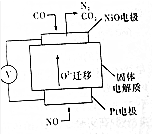
�ٲ�˿�缫Ϊ���������������������
�ڸ�����ӦʽΪCO+O2--2e-=CO2��
��1����֪2SO2��g��+O2��g��?2SO3��g���ǹ�ҵ������Ĺؼ���Ӧ����ͼ1Ϊ��ͬ�¶ȣ�T1��T2����SO2��ת������ʱ��ı仯���ߣ�
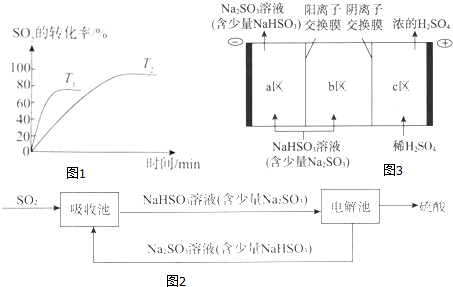
��T1�����������������=����T2���жϵ��������¶�Խ�߷�Ӧ����Խ�죬�ﵽ��ѧƽ���ʱ��Խ�̣��÷�ӦΪ�ţ���š����������ȷ�Ӧ���жϵ��������¶�����ʱƽ�������ȷ����ƶ���SO2��ת���ʼ�С��
�����Ϊһ���¶Ⱥ�ѹǿ�£�4��Ͷ�ϱ�[n��SO2����n��O2��]�ֱ�Ϊ2��18��4��15��7��11��8��10ʱSO2��ƽ��ת���ʣ�
| Ͷ�ϱ� | a | b | c | d |
| SO2ƽ��ת����/% | 97.1 | 96.8 | 95.8 | 90.0 |
ii��Ͷ�ϱ�Ϊ8��10ʱ��ƽ����������SO3�������Ϊ50%��
��2���Ƽ�ѭ�����������᳧β���е�SO2������ת��Ϊ����Ĺ�����ͼ2��
�����ճ��з�����Ӧ�����ӷ���ʽ��SO2+SO32-+H2O=2HSO3-��
�ڵ��صĹ���ʾ��ͼ��ͼ3��
i����ͼ�б�ʾ��b����Na+��HSO3-���ƶ�����
ii����������H2SO4�ĵ缫��Ӧʽ˵��c�����õ�Ũ�������⣬����õ�ʲô���ʣ�SO2��
| A�� | p ��Ne����p ��H2����p ��O2�� | B�� | p ��O2����p ��Ne����p ��H2�� | C�� | p ��H2����p ��O2����p ��Ne�� | D�� | p ��H2����p ��Ne����p ��O2�� |
| A�� | �Ȼ�ȩ������Br2�����ӳɷ�Ӧ | |
| B�� | �Ȼ�ȩ�ܷ���������Ӧ | |
| C�� | 1 mol�Ȼ�ȩ��������2 mol H2�����ӳɷ�Ӧ | |
| D�� | �Ȼ�ȩ����ϩ��ͬϵ�� |
 2010�����˻����ҹ����ݳɹ��ٰ죬�������˻������˻������
2010�����˻����ҹ����ݳɹ��ٰ죬�������˻������˻������