题目内容
某有机物链状分子中含a个甲基,n个亚甲基( ),m个次甲基(
),m个次甲基(  ),其余为羟基.则羟基的个数为( )
),其余为羟基.则羟基的个数为( )
 ),m个次甲基(
),m个次甲基(  ),其余为羟基.则羟基的个数为( )
),其余为羟基.则羟基的个数为( )| A、m+2-a |
| B、m-a |
| C、2n+3m-a |
| D、m+2n+2-a |
考点:常见有机化合物的结构
专题:
分析:有机物主要靠C原子连接,每个碳原子都必须形成4个共价键,以1条碳链分析考虑,先分析若只连接甲基,计算连接的甲基数目,再根据分子中含有的甲基数目计算羟基数.1个-CH-可连接1个甲基,-CH2-不管多少个只能连接两个-CH3.据此计算判断.
解答:
解:若只连接甲基,-CH2-不管多少个只能连接两个-CH3,m个-CH-,能连接m个-CH3,所以n个-CH2-,m个-CH-,连接-CH3共计m+2个.由于分子中含有a个-CH3,所以连接的-OH为m+2-a,故选A.
点评:本题考查有机化合物中成键特征,难度中等,关键清楚有机物主要靠C原子连接,每个碳原子都必须形成4个共价键.

练习册系列答案
相关题目
下列有关说法正确的是( )
| A、镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | ||
| B、已知某温度下:Ksp(AgCl)=1.8×10-10、Ksp(Ag2CrO4)=1.2×-12,所以该温度下AgCl的溶解度大于Ag2CrO | ||
C、室温下,将浓度为0.1mol/LHF溶液加水稀释,其电离平衡常数和
| ||
| D、反应3NO2(g)+H2O═2HNO3+NO在室温下可自发进行,则该反应的△H>0 |
在水中存在H2O?H++OH-平衡,加入下列哪种物质或进行哪项操作,不会使平衡发生移动( )
| A、加入NaOH |
| B、加入CH3COOH |
| C、加入NaCl |
| D、升温 |
 固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )| A、有O2放电的a极为电池的负极 |
| B、a极对应的电极反应为:O2+2H2O+4e-=4OH- |
| C、有H2放电的一极电极反应为:H2+O2--2e-=H2O |
| D、该电池的总反应方程式为:2H2+O2=2H2O |
根据元素周期律,碱金属元素的下列性质从上到下依次递增的有( )
| A、金属性 | B、化合价 |
| C、原子半径 | D、单质的还原性 |
下列有关反应热的说法中正确的是( )
| A、一个化学反应是否能在常温下发生与该反应的△H值的大小没有必然联系 |
| B、中和热△H=-57.3kJ?mol-1,所以1.00L 1.00mol?L-1H2SO4与稀的NaOH溶液恰好完全反应放出57.3kJ的热量 |
| C、需要加热才能发生的反应一定是吸热反应 |
| D、在101KPa时,1molCH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热 |
下列物质中,属于由分子组成的纯净化合物的是( )
| A、干冰 | B、石墨 |
| C、二氧化硅 | D、聚氯乙烯 |
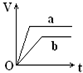
 向足量的a、b两份锌粉中,分别加入少量且等量的稀H2SO4,同时向a中加入少量的CuSO4溶液.如图表示产生H2的体积(V)与时间(t)的关系,其中正确的是( )
向足量的a、b两份锌粉中,分别加入少量且等量的稀H2SO4,同时向a中加入少量的CuSO4溶液.如图表示产生H2的体积(V)与时间(t)的关系,其中正确的是( )