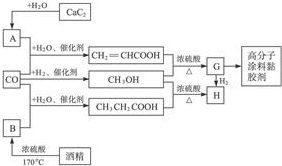
题目内容
16.常愠下铝制容器或铁制容器可贮运浓硫酸,这利用了浓硫酸的( )| A. | 强酸性 | B. | 吸水性 | C. | 脱水性 | D. | 强氧化性 |
分析 常温下铝制容器或铁制容器可贮运浓硫酸,表面形成致密的氧化膜,发生钝化现象,体现浓硫酸的强氧化性,由此分析解答.
解答 解:常温下铝制容器或铁制容器可贮运浓硫酸,表面形成致密的氧化膜,发生钝化现象,体现浓硫酸的强氧化性,故选D.
点评 本题考查了浓硝酸和浓硫酸的性质,知道二者都具有强氧化性,常温下能与铁或铝发生钝化现象,知道二者性质的差异性,题目难度不大.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
6.下列叙述正确的是( )
| A. | 棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O | |
| B. | 清洁能源所用光电池的生产材料主要是用高纯度的二氧化硅 | |
| C. | 在医疗上氢氧化铝可用于治疗胃酸过多 | |
| D. | 漂白粉在使用时一定要加入一定量的盐酸才能起到漂白作用 |
1.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.其中Z所处的周期序数与族序数相等.下列说法不正确的是( )
| X | Y | Q | ||
| Z | W |
| A. | 形成简单离子的半径大小顺序:r(W)>r(Z)>r(Y) | |
| B. | 最简单气态氢化物的热稳定性:Y>X | |
| C. | Q的氢化物的水溶液可用于蚀刻玻璃 | |
| D. | X、Z的最高价氧化物均可与NaOH溶液反应 |
8.下列有关化学用语表示正确的是( )
| A. | 质子数为53、中子数为78的碘原子:${\;}_{53}^{131}$I | |
| B. | 硫离子的结构示意图: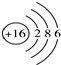 | |
| C. | H2O2的结构式:H-O-H-O | |
| D. | NH4I的电子式: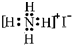 |
5.向FeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤沉淀,然后在空气中灼烧沉淀,最终得到的固体物质是( )
| A. | Fe2O3 | B. | FeO | C. | Fe(OH)3 | D. | Fe3O4 |
6.“神舟”飞船成功发射,标志着我国航天科技达到了较高水平.为了降低宇航员所在轨道舱和返回舱内二氧化碳的浓度,同时释放氧气,舱内放入下列哪种物质能满足上述要求( )
| A. | H2O | B. | Na2O2 | C. | KClO3 | D. | KMnO4 |