题目内容
已知标准状况下1体积水溶解了560体积氨气,所得氨水的密度为0.9g/cm3,试求该氨水的质量分数和物质的量浓度.
考点:溶液中溶质的质量分数及相关计算,物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:NH3溶于水后虽然大部分生成NH3?H2O,但在计算时,仍以NH3作为氨水中的溶质,设水的体积为1L,则氨气的体积为560L,根据n=
计算氨气的物质的量,根据m=nM计算氨气质量,根据m=ρV计算水的质量,溶液质量=氨气质量+水的质量,根据质量分数=
×100%计算该氨水的质量分数,再根据c=
计算氨水的物质的量浓度.
| m |
| M |
| 溶质质量 |
| 溶液质量 |
| 1000ρω |
| M |
解答:
解:NH3溶于水后虽然大部分生成NH3?H2O,但在计算时,仍以NH3作为氨水中的溶质;
设水的体积为1L,氨气的体积为560L,
则氨气的物质的量为=
=25mol,
氨气的质量为25mol×17g/mol=425g,
1L水的质量=1L×1000g/L=1000g,
溶液的质量为1000g+425mol=1425g,
则氨水的质量分数为w=
×100%=29.8%,
氨水的物质的量浓度为c=
mol/L=15.8 mol/L,
答:该氨水的质量分数为29.8%、物质的量浓度为15.8mol/L.
设水的体积为1L,氨气的体积为560L,
则氨气的物质的量为=
| 560L |
| 22.4L/mol |
氨气的质量为25mol×17g/mol=425g,
1L水的质量=1L×1000g/L=1000g,
溶液的质量为1000g+425mol=1425g,
则氨水的质量分数为w=
| 425g |
| 1425g |
氨水的物质的量浓度为c=
| 1000×0.9×29.8% |
| 17 |
答:该氨水的质量分数为29.8%、物质的量浓度为15.8mol/L.
点评:本题考查物质的量浓度和质量分数的计算,难度中等,注意理解掌握物质的量浓度与质量分数之间关系,可以利用定义法计算溶液物质的量浓度,计算溶液的体积是关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
一定温度下,在密闭容器中发生如下反应:2A?2B(g)+C,关于该反应速率的说法正确的是( )
| A、增加A的物质的量,正反应速率一定增大 |
| B、升高温度正逆反应速率均增大 |
| C、保持容器体积不变充入稀有气体,若反应速率不变说明A是气体,C为非气体 |
| D、若改变条件使正反应速率减小,则逆反应速率也一定减小 |
下列数字表示元素的原子序数,其中包含金属、非金属、稀有气体元素各一种的是( )
| A、3、16、20 |
| B、2、4、18 |
| C、11、15、18 |
| D、9、10、17 |
在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,n(SO2)随时间的变化如表:则下列说法正确的是( )
| 时间/min | 0 | 1 | 2 | 3 | 4 | 3 |
| n(SO2)/mol | 0.20 | 0.1 6 | 0.13 | 0.11 | 0.08 | 0.08 |
| A、当v(SO2)=v(SO3)时,说明该反应已达到平衡状态 |
| B、平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大 |
| C、若升高温度,则SO2的反应速率会变大,平衡常数K值会增大 |
| D、用O2表示0~4min内该反应的平均速率为0.005mol/(L?min) |
 某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样3.52克置于铂舟并放入燃烧管中,不断通入氧气流.用酒精喷灯持续加热样品,将生成物先后通过无水硫酸铜和碱石灰,两者分别增重1.44克和5.28克,生成物完全被吸收.试回答以下问题:
某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样3.52克置于铂舟并放入燃烧管中,不断通入氧气流.用酒精喷灯持续加热样品,将生成物先后通过无水硫酸铜和碱石灰,两者分别增重1.44克和5.28克,生成物完全被吸收.试回答以下问题:

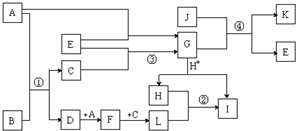 如图中各物质均为中学化学中的常见物质,其中A、E、J三种物质为单质,D的摩尔质量比F小16,F为红棕色气体;K是一种两性氧化物,可用KSCN检验I中的阳离子.它们的相互转化关系如图所示(图中部分产物、反应条件未列出).
如图中各物质均为中学化学中的常见物质,其中A、E、J三种物质为单质,D的摩尔质量比F小16,F为红棕色气体;K是一种两性氧化物,可用KSCN检验I中的阳离子.它们的相互转化关系如图所示(图中部分产物、反应条件未列出).