题目内容
12.在农业上,尿素CO(NH2)2、NH4NO3、NH4HCO3、(NH4)2CO3都可以做氮肥使用.在这四种物质中,氮的质量分数最高的是( )| A. | 尿素CO(NH2)2 | B. | NH4NO3 | C. | NH4HCO3 | D. | (NH4)2CO3 |
分析 将NH4HCO3转化为(NH4)2(HCO3)2,N元素质量分数不变,各化学式中N原子数目相等,则相对分子质量越小N元素质量分数越大.
解答 解:将NH4HCO3转化为(NH4)2(HCO3)2,N元素质量分数不变,各化学式中N原子数目相等,由N元素质量分数=$\frac{N原子总相对原子质量}{相对分子质量}$可知,相对分子质量越小N元素质量分数越大,CO(NH2)2、NH4NO3、(NH4)2(HCO3)2、(NH4)2CO3,的相对分子质量依次为60、80、158、96,故尿素CO(NH2)2中氮的质量分数最高,
故选A.
点评 本题考查质量分数有关计算,难度不大,注意对质量分数概念的理解与灵活应用.

练习册系列答案
相关题目
2.相同物质的量的Na2O2和Na2O 的比较中,不正确的是( )
| A. | 两种物质所含原子个数之比为4:3 | |
| B. | 两种物质与水充分反应,生成的氢氧化钠质量之比为2:1 | |
| C. | 两种物质与足量的CO2反应,消耗气体的质量比为1:1 | |
| D. | 两种物质中阳离子的物质的量之比为1:1 |
20.某气体的摩尔质量为M g/mol,NA表示阿伏加德罗常数,在一定的温度和压强下,体积为V L的该气体所含有的分子数为X.则$\frac{MX}{V{N}_{A}}$表示的是( )
| A. | V L该气体的质量(以g为单位) | B. | 1 L该气体的质量(以g为单位) | ||
| C. | 1 mol该气体的体积(以L为单位) | D. | 1 L该气体的物质的量(以mol为单位) |
4.25℃时,将氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是( )
| A. | [NH4+]=[SO42-] | B. | [NH4+]>[SO42-] | ||
| C. | [NH4+]<[SO42-] | D. | [OH-]+[SO42-]=[H+]+[NH4+] |
1.在一密闭容器中有CO、H2、O2共8.5g和足量的Na2O2,用电火花引燃,使其完全反应,Na2O2增重4.9g,则原混合气体中O2的质量分数是( )
| A. | 57.6% | B. | 42.4% | C. | 53.6% | D. | 46.4% |
2.用NA代表阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 16g氧气中所含的氧原子数为NA | |
| B. | 1molCl2与足量H2O反应,转移的电子数为2NA | |
| C. | 标准状况下,22.4L二氧化硅所含有的原子数目为3NA | |
| D. | 钠在氧气中燃烧,1 mol O2作氧化剂时得到的电子数为4NA |
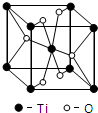 第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.
第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.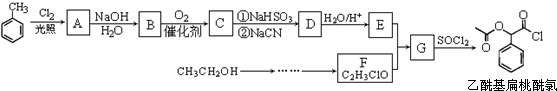
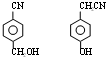
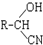 ,RCN$\stackrel{H_{2}O/H+}{→}$RCOOH,RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′
,RCN$\stackrel{H_{2}O/H+}{→}$RCOOH,RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′ ,E中含氧官能团的名称醇羟基和羧基.
,E中含氧官能团的名称醇羟基和羧基.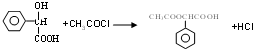 .
. .
.