题目内容
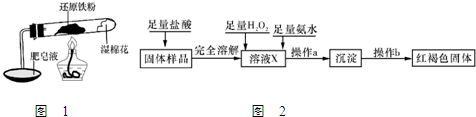
把苯酚晶体加入试管内的热水中得澄清的溶液,把试管浸入冷水中,溶液变浑浊,这是因为
苯酚在冷水中溶解度减小
苯酚在冷水中溶解度减小
.再往试管内滴入氢氧化钠溶液又变澄清,其反应方程式是:C6H5OH+NaOH═C6H5ONa+H2O
C6H5OH+NaOH═C6H5ONa+H2O
.盛过苯酚的容器用乙醇
乙醇
清洗.分离苯和苯酚的混合物,所加试剂为氢氧化钠溶液
氢氧化钠溶液
,主要分离方法为分液
分液
.分析:苯酚在水中的溶解度随温度的升高而增大,在冷水中溶解度减小,溶液会变浑浊;苯酚具有弱酸性,能够与氢氧化钠溶液反应生成苯酚钠与水;苯酚易溶于乙醇等有机溶剂,盛过苯酚的容器用乙醇清洗;分离苯和苯酚的混合物,用NaOH溶液反应后再分液.
解答:解:由于苯酚在水中的溶解度随温度的升高而增大,在冷水中溶解度减小,溶液会变浑浊,
苯酚具有弱酸性,能够与氢氧化钠溶液反应生成苯酚钠与水,反应的化学方程式为:C6H5OH+NaOH═C6H5ONa+H2O,
苯酚易溶于乙醇等有机溶剂,盛过苯酚的容器用乙醇清洗;分离苯和苯酚的混合物,用NaOH溶液反应后再分液,
故答案为:苯酚在冷水中溶解度减小;C6H5OH+NaOH═C6H5ONa+H2O;乙醇;氢氧化钠溶液;分液.
苯酚具有弱酸性,能够与氢氧化钠溶液反应生成苯酚钠与水,反应的化学方程式为:C6H5OH+NaOH═C6H5ONa+H2O,
苯酚易溶于乙醇等有机溶剂,盛过苯酚的容器用乙醇清洗;分离苯和苯酚的混合物,用NaOH溶液反应后再分液,
故答案为:苯酚在冷水中溶解度减小;C6H5OH+NaOH═C6H5ONa+H2O;乙醇;氢氧化钠溶液;分液.
点评:本题考查了苯酚的性质,注重了基础知识考查,苯酚又名石碳酸,具有弱酸性,能够与氢氧化钠溶液反应,本题难度不大.

练习册系列答案
相关题目
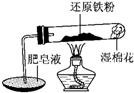 已知在温度低于570℃时,还原铁粉与水蒸气反应的产物是FeO,高于570℃时,生成Fe3O4.老师用图示实验装置,完成了还原铁粉与水蒸气反应的演示实验.
已知在温度低于570℃时,还原铁粉与水蒸气反应的产物是FeO,高于570℃时,生成Fe3O4.老师用图示实验装置,完成了还原铁粉与水蒸气反应的演示实验.甲同学为探究实验后试管内的固体含有哪些物质,进行了下列实验:
| 实验 编号 |
实验操作 | 实验现象 |
| ① | 取少量黑色粉末放入试管中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
| ② | 向试管中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
| A、试管内的固体一定含有铁粉 |
| B、试管内的固体一定不含有Fe3O4 |
| C、不能确定试管内的固体一定含有FeO |
| D、可通过将试管内固体彻底还原,分析其质量减小的方法来确定是否含有Fe3O4 |