题目内容
某化学反应的能量变化如图所示.下列有关叙述正确的是( )


| A、该反应为放热反应 |
| B、E2可表示形成新的化学键所释放的能量 |
| C、该反应的反应热△H=E1-E2 |
| D、加入催化剂可同等程度的降低E1、E2 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、根据反应物的总能量比生成物的总能量小来判断;
B、E2可表示断裂反应物所吸收的热量;
C、根据焓变的概念△H=产物的总焓-反应物的总焓来回答;
D、催化剂能降低反应的活化能,从而加快化学反应速率,不会改变化学反应的焓变.
B、E2可表示断裂反应物所吸收的热量;
C、根据焓变的概念△H=产物的总焓-反应物的总焓来回答;
D、催化剂能降低反应的活化能,从而加快化学反应速率,不会改变化学反应的焓变.
解答:
解:A、因为由图象反应物的总能量比生成物的总能量小,所以该反应为吸热反应,故A错误;
B、E2可表示断裂反应物所吸收的热量,故B错误;
C、焓变△H=产物的总焓-反应物的总焓=△H=E2-E1,故C错误;
D、催化剂会降低反应的活化能,从而加快化学反应速率,不会改变化学反应的焓变,所以加入催化剂可同等程度的降低E1、E2,故D正确;
故选D.
B、E2可表示断裂反应物所吸收的热量,故B错误;
C、焓变△H=产物的总焓-反应物的总焓=△H=E2-E1,故C错误;
D、催化剂会降低反应的活化能,从而加快化学反应速率,不会改变化学反应的焓变,所以加入催化剂可同等程度的降低E1、E2,故D正确;
故选D.
点评:本题考查了反应能量变化的分析判断,图象分析是解题关键,反应的能量守恒是判断的依据,注意加入催化剂不会改变化学反应的焓变,会降低反应的活化能.

练习册系列答案
相关题目
在一定温度下,向容积固定的密闭容器里充入a mol N2O4发生如下反应:N2O4 (气)?2NO2 (气),达到平衡后,再向该容器内充入a mol N2O4,达平衡后与原平衡比较正确的是( )
| A、平均相对分子质量减小 |
| B、N2O4的转化率提高 |
| C、压强为原来的2倍 |
| D、颜色变深 |
常温下,某无色透明的溶液中,下列各组离子能够大量共存的是( )
| A、H+、Na+、Cl-、CO32- |
| B、Ba2+、Na+、SO42-、Cl- |
| C、MnO4-、K+、I-、H+ |
| D、Mg2+、Cl-、NO3-、H+ |
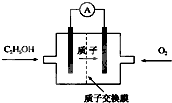 目前已研制出一种用磺酸类质子作溶剂的酸 性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )
目前已研制出一种用磺酸类质子作溶剂的酸 性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )| A、通入乙醇的电极为该电池的正极 |
| B、放电过程中,电源内部的H+从正极区向负极区迁移 |
| C、该电池的正极反应为:4H++O2+4e-=2H2O |
| D、用该电池做电源,用惰性电极电解饱和NaCl溶液时,每消耗0.2 mol C2H5OH,阴极产生标准状况下气体的体积为13.44 L |
下列条件下,两瓶气体所含原子数一定相等的是( )
| A、同压强、同温度的O2和O3 |
| B、同温度、同体积的NH3和N2 |
| C、同体积、同密度的C2H4和C3H6 |
| D、同压强、同体积的N2O和CO2 |
在离子浓度都为0.1mol/L的下列溶液中,加入(或通入)某物质后,发生反应先后顺序正确的是( )
| A、在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B、在含I-、SO32-、Br-的溶液中不断通入氯气:I-、Br-、SO32- |
| C、在含Fe3+、H+、NH4+的溶液中逐滴加入烧碱溶液:Fe3+、NH4+、H+ |
| D、在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32- |
需加入氧化剂才能实现的是( )
| A、Fe3+→Fe2+ |
| B、Cl-→Cl2 |
| C、CuO→Cu |
| D、H2SO4→BaSO4 |