题目内容
把18.0mol?L-1的浓硫酸稀释成2.00mol?L-1的稀硫酸100ml,实验操作如下:
A.将配好的稀硫酸倒入试剂瓶中,贴好标签;
B.盖好容量瓶塞,反复颠倒,摇匀;
C.用量筒量取 ml的18.0mol?L-1的浓硫酸;
D.将 沿烧杯内壁慢慢注入盛有少量 的烧杯中;
E.用少量蒸馏水洗涤烧杯2-3次,并将洗涤液也全部转移到容量瓶中;
F.将已冷却至室温的硫酸溶液沿玻璃棒注入 mL的容量瓶中;
G.改用胶头滴管逐滴加蒸馏水,使溶液凹面恰好与刻度相切;
H.继续向容量瓶中加蒸馏水,直到液面接近刻度线 cm处.
(1)填写上述步骤中的空白:C ;D F H .
(2)请按正确的操作步骤进行排序 .
(3)试分析下列操作会使所配溶液的浓度是大于还是小于、等于2.00mol?L-1浓度?
①若在操作中没有把少量蒸馏水洗涤烧杯的洗涤液全部转移到容量瓶中,会使稀硫酸溶液的浓度
(大于,小于,等于)2.00mol?L-1.
②若容量瓶未干燥即用来配制溶液, (大于,小于,等于)2.00mol?L-1.
③若定容时俯视刻度线,会使稀硫酸溶液的浓度 (大于,小于,等于)2.00mol?L-1.
A.将配好的稀硫酸倒入试剂瓶中,贴好标签;
B.盖好容量瓶塞,反复颠倒,摇匀;
C.用量筒量取
D.将
E.用少量蒸馏水洗涤烧杯2-3次,并将洗涤液也全部转移到容量瓶中;
F.将已冷却至室温的硫酸溶液沿玻璃棒注入
G.改用胶头滴管逐滴加蒸馏水,使溶液凹面恰好与刻度相切;
H.继续向容量瓶中加蒸馏水,直到液面接近刻度线
(1)填写上述步骤中的空白:C
(2)请按正确的操作步骤进行排序
(3)试分析下列操作会使所配溶液的浓度是大于还是小于、等于2.00mol?L-1浓度?
①若在操作中没有把少量蒸馏水洗涤烧杯的洗涤液全部转移到容量瓶中,会使稀硫酸溶液的浓度
②若容量瓶未干燥即用来配制溶液,
③若定容时俯视刻度线,会使稀硫酸溶液的浓度
考点:配制一定物质的量浓度的溶液
专题:
分析:(1)C、根据溶液的稀释定律C浓V浓=C稀V稀来计算;
D、根据浓硫酸的稀释放热来分析;
F、容量瓶只有一条刻度线,故只能配制出与其规格相对应的体积的溶液,据此来选择容量瓶的规格;
H、根据定容的操作来分析;
(2)根据操作过程是计算、量取、稀释、移液、洗涤、定容、摇匀、装瓶等步骤来排序;
(3)根据C=
,通过判断不当操作对溶质的物质的量n和溶液体积V的影响来分析误差.
D、根据浓硫酸的稀释放热来分析;
F、容量瓶只有一条刻度线,故只能配制出与其规格相对应的体积的溶液,据此来选择容量瓶的规格;
H、根据定容的操作来分析;
(2)根据操作过程是计算、量取、稀释、移液、洗涤、定容、摇匀、装瓶等步骤来排序;
(3)根据C=
| n |
| V |
解答:
解:(1)C、设需要的浓硫酸的体积为VmL,根据溶液的稀释定律C浓V浓=C稀V稀可知:
18mol/L×VmL=2mol/L×100mL
解得V=11.1mL,故答案为:11.1;
D、由于浓硫酸的稀释放热,故要将浓硫酸沿烧杯内壁注入水中,故答案为:浓硫酸,水;
F、容量瓶只有一条刻度线,故只能配制出与其规格相对应的体积的溶液,故配制100mL溶液应选择100mL容量瓶,故答案为:100;
H、定容时,先向容量瓶中加水至液面离刻度线1-2cm处,改用胶头滴管加水,故答案为:1-2;
(2)根据操作过程是计算、量取、稀释、移液、洗涤、定容、摇匀、装瓶等步骤来排序可知:正确的操作顺序是:C D F E H G B A,故答案为:C D F E H G B A;
(3)①若在操作中没有把少量蒸馏水洗涤烧杯的洗涤液全部转移到容量瓶中,会导致溶质的损失,则会使稀硫酸溶液的浓度偏小,故答案为:小于;
②只要最后定容时凹液面与刻度线相切即可,至于水是事先就有的还是后来加入的,对浓度无影响,故答案为:等于;
③若定容时俯视刻度线,会导致溶液体积偏小,则浓度偏高,故答案为:大于.
18mol/L×VmL=2mol/L×100mL
解得V=11.1mL,故答案为:11.1;
D、由于浓硫酸的稀释放热,故要将浓硫酸沿烧杯内壁注入水中,故答案为:浓硫酸,水;
F、容量瓶只有一条刻度线,故只能配制出与其规格相对应的体积的溶液,故配制100mL溶液应选择100mL容量瓶,故答案为:100;
H、定容时,先向容量瓶中加水至液面离刻度线1-2cm处,改用胶头滴管加水,故答案为:1-2;
(2)根据操作过程是计算、量取、稀释、移液、洗涤、定容、摇匀、装瓶等步骤来排序可知:正确的操作顺序是:C D F E H G B A,故答案为:C D F E H G B A;
(3)①若在操作中没有把少量蒸馏水洗涤烧杯的洗涤液全部转移到容量瓶中,会导致溶质的损失,则会使稀硫酸溶液的浓度偏小,故答案为:小于;
②只要最后定容时凹液面与刻度线相切即可,至于水是事先就有的还是后来加入的,对浓度无影响,故答案为:等于;
③若定容时俯视刻度线,会导致溶液体积偏小,则浓度偏高,故答案为:大于.
点评:本题考查了一定物质的量浓度溶液的配制以及误差分析,难度不大,注意实验的基本操作方法和注意事项.

练习册系列答案
相关题目
对于反应2NO(g)+O2(g)?2NO2(g)△H<0,达到平衡后升高温度,则( )
| A、平衡正向移动 |
| B、平衡逆向移动 |
| C、反应速率减小 |
| D、正反应速率减小 |
下列两种气体的分子数一定相等的是( )
| A、质量相等、密度不等的N2和C2H4 |
| B、等体积等密度的CO和C2H4 |
| C、等温等体积的O3和N2 |
| D、等压等体积的N2和CO2 |
2005年2月18日,英国食品标准局向英国民众发出警告,公布了359种食品中含有可能致癌的“苏丹红一号”,一时间“苏丹红一号”成为媒体关注的焦点.“苏丹红一号”的结构简式如图下列关于苏丹红一号的有关叙述正确的是( )
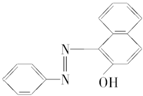

| A、苏丹红一号的分子式C18H12N2O |
| B、苏丹红一号的相对分子质量是248 g?mol-1 |
| C、苏丹红一号属于烃 |
| D、苏丹红一号能发生加成反应 |
下列叙述正确的是( )
| A、乙烯和苯都能够使溴水褪色,褪色的原因相同 |
| B、淀粉、油脂、蛋白质都能够发生水解,且都能生成二种产物 |
| C、煤油可由石油分馏获得,可用作燃料和保存少量金属 |
| D、乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用Na OH溶液除去 |
有关AgCl沉淀的溶解平衡的说法正确的是( )
| A、AgCl沉淀的生成和溶解在达到平衡时就不再进行 |
| B、AgCl不溶于水,溶液中没有Cl-和Ag+ |
| C、升高温度,AgCl的溶解度增大,Ksp增大 |
| D、向AgCl饱和溶液中加入NaCl固体,AgCl的溶解度和Ksp都不变 |
X、Y、Z、W、Q都是短周期元素,其中X原子的最外层电子数是内层电子数的3倍;X与Z同族,Y与Z同周期,Q原子的电子总数等于其电子层数的3倍,W与X、Y既不同族也不同周期且W不为稀有气体元素;X、Y、Z三种元素的族序数之和为16.下列说法正确的是( )
| A、Q与W能形成10电子,不能形成14电子、18电子分子 |
| B、Y的最高价氧化物对应水化物的化学式只能表示为H4YO4 |
| C、Y、Z、Q分别与X化合,只能形成AB2型化合物 |
| D、X、Z、W中的两种或三种元素形成的钠盐溶液可能显酸性、碱性、中性 |
化学与生活、社会密切相关.下列说法不正确的是( )
| A、乙醇是一种再生能源,充分燃烧的产物不污染环境 |
| B、凡含有食品添加剂的食物对人体健康均有害,不可食用 |
| C、为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
| D、提倡人们购物时不用塑料袋,是为了防止白色污染 |