题目内容
5.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3- | |
| B. | 0.1 mol/L的AlCl3溶液中:Na+、K+、SO42-、HCO3- | |
| C. | 25℃时,水电离出的c(H+)=1×l0-l3 mol/L的溶液中:K+、Ba2+、NO3-、S2- | |
| D. | 能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl- |
分析 A.能溶解Al(OH)3的溶液为酸性或强碱性溶液,铵根离子与氢氧根离子反应,碳酸氢根离子与氢离子、氢氧根离子反应;
B.氯化铝电离出的铝离子与碳酸氢根离子发生双水解反应;
C.25℃时,水电离出的c(H+)=1×l0-l3 mol/L的溶液中存在大量氢离子或氢氧根离子,硝酸根离子在酸性条件下氧化硫离子;
D.能使酚酞变红的溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应.
解答 解:A.能溶解Al(OH)3的溶液中存在大量氢离子或氢氧根离子,HCO3-与氢离子和氢氧根离子反应,NH4+与氢氧根离子反应,在溶液中一定不能大量共存,故A错误;
B.AlCl3、HCO3-之间发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,在溶液中不能大量共存,故B错误;
C.25℃时,水电离出的c(H+)=1×l0-l3 mol/L的溶液为酸性或碱性溶液,酸性条件下NO3-、S2-之间发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.能使酚酞变红的溶液为碱性溶液,溶液中存在大量氢氧根离子,Na+、Ba2+、NO3-、Cl-之间不发生反应,都不与氢氧根离子反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
15.锰的用途非常广泛,在钢铁工业中,锰的用量仅次于铁,90%的锰消耗于钢铁工业,10%的锰消耗于有色冶金、化工、电子、电池、农业等部门.以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴等碳酸盐杂质)为原料生产金属锰的工艺流程如下:

已知25℃,部分物质的溶度积常数如下:
(1)步骤Ⅰ中,MnCO3与硫酸反应的化学方程式是MnCO3+H2SO4=MnSO4+CO2↑+H2O;
(2)步骤Ⅰ中需要加入稍过量的硫酸,其目的有3点:①使矿物中的物质充分反应;②提供第Ⅱ步氧化时所需要的酸性环境;③抑制Mn2+的水解;
(3)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+氧化为Fe3+,该反应的离子方程式是MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
加氨水调节溶液的pH为5.0~6.0,以除去Fe3+.
(4)步骤Ⅲ中,需要用到的玻璃仪器除玻璃棒、漏斗外,还有烧杯;滤渣2的主要成分是CoS和NiS;
(5)电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降.欲使溶液中c(Mn2+)≤1.0×10-5 mol•L-1,则应保持溶液中c(S2-)≥1.0×10-6 mol•L-1.

已知25℃,部分物质的溶度积常数如下:
| 物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(2)步骤Ⅰ中需要加入稍过量的硫酸,其目的有3点:①使矿物中的物质充分反应;②提供第Ⅱ步氧化时所需要的酸性环境;③抑制Mn2+的水解;
(3)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+氧化为Fe3+,该反应的离子方程式是MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
加氨水调节溶液的pH为5.0~6.0,以除去Fe3+.
(4)步骤Ⅲ中,需要用到的玻璃仪器除玻璃棒、漏斗外,还有烧杯;滤渣2的主要成分是CoS和NiS;
(5)电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降.欲使溶液中c(Mn2+)≤1.0×10-5 mol•L-1,则应保持溶液中c(S2-)≥1.0×10-6 mol•L-1.
16.下列实验操作或装置(略去部分夹持仪器)正确的是( )
| A. | 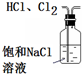 除去HCl中含有的少量Cl2 | B. | 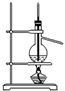 石油的蒸馏 | ||
| C. |  制备乙酸乙酯 | D. |  制备收集干燥的氨气 |
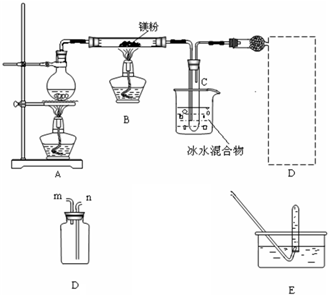
13. 如图所示,打开分液漏斗后,加热,烧杯中出现黄色沉淀并有臭鸡蛋气味的气体逸出,则原烧杯中n(Na2S)与n(Na2SO3)的比值需满足( )
如图所示,打开分液漏斗后,加热,烧杯中出现黄色沉淀并有臭鸡蛋气味的气体逸出,则原烧杯中n(Na2S)与n(Na2SO3)的比值需满足( )
 如图所示,打开分液漏斗后,加热,烧杯中出现黄色沉淀并有臭鸡蛋气味的气体逸出,则原烧杯中n(Na2S)与n(Na2SO3)的比值需满足( )
如图所示,打开分液漏斗后,加热,烧杯中出现黄色沉淀并有臭鸡蛋气味的气体逸出,则原烧杯中n(Na2S)与n(Na2SO3)的比值需满足( )| A. | >2 | B. | <2 | C. | =2 | D. | 1~2之间 |
10.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | c(OH-)=0.1mol/L的溶液:Na+、K+、CO32-、ClO- | |
| B. | 滴入酚酞显红色的溶液中:Na+、Al3+、CO32-、AlO2- | |
| C. | 含有Fe3+的溶液中:Na+、Al3+、Cl-、SCN- | |
| D. | pH=1的溶液中:Fe2+、Cl-、NO3-、K+ |
17. 屠呦呦因对青蒿素的研究而获得诺贝尔生理学或医学奖,青蒿素可以青蒿酸(结构简式如图所示)为原料合成,下列关于青蒿酸的说法中正确的是( )
屠呦呦因对青蒿素的研究而获得诺贝尔生理学或医学奖,青蒿素可以青蒿酸(结构简式如图所示)为原料合成,下列关于青蒿酸的说法中正确的是( )
 屠呦呦因对青蒿素的研究而获得诺贝尔生理学或医学奖,青蒿素可以青蒿酸(结构简式如图所示)为原料合成,下列关于青蒿酸的说法中正确的是( )
屠呦呦因对青蒿素的研究而获得诺贝尔生理学或医学奖,青蒿素可以青蒿酸(结构简式如图所示)为原料合成,下列关于青蒿酸的说法中正确的是( )| A. | 分子式为C15H24O2 | B. | 属子芳香族化合物 | ||
| C. | 能发生取代反应和加成反应 | D. | 分子中所有原子可能共平面 |

 .
. .
. 的合成路线(无机原料任选).
的合成路线(无机原料任选).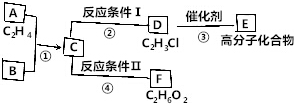 已知:
已知: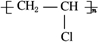 ,FCH2OHCH2OH.
,FCH2OHCH2OH.