题目内容
1.下列物质中,不能用单质直接化合制得的是( )| A. | CuCl2 | B. | FeCl2 | C. | MgCl2 | D. | Fe3O4 |
分析 氯气具有强氧化性,氯气与变价金属反应生成高价金属氯化物,铁与氧气反应生成四氧化三铁,以此来解答.
解答 解:A.Cu与氯气发生化合反应生成CuCl2,故A不选;
B.Fe与氯气发生化合反应生成FeCl3,故B选;
C.Mg与氯气发生化合反应生成MgCl2,故C不选;
D.Fe与氧气发生化合反应生成Fe3O4,故D不选;
故选B.
点评 本题考查金属及化合物的性质,为高频考点,把握物质的性质、发生的氧化还原反应为解答的关键,侧重分析与应用能力的考查,注意氯气的强氧化性,题目难度不大.

练习册系列答案
相关题目
13.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温下,1.0 L 1.0 mol•L-1KAlO2溶液中含有的氧原子数为2 NA | |
| B. | 7.8 g Na2O2固体中含有的阴离子数为0.2 NA | |
| C. | 标准状况下,体积为2.24 L的CO2和SO2的混合气体中含有的氧原子数为0.2 NA | |
| D. | 0.1 mol Cl2参加氧化还原反应,转移的电子数目一定是0.2 NA |
9.下列有关混合物的分离与提纯的说法正确的是( )
| A. | 由于碘在乙醇中的溶解度较大,所以可用乙醇把碘水中的碘萃取出来 | |
| B. | 可用加热蒸馏的方法使含水乙醇变为无水乙醇 | |
| C. | 由于汽油和水不互溶,因此可用分液的方法将二者分离 | |
| D. | NaCl的溶解度随温度下降而减小,所以用冷却法从热的含少量KNO3的NaCl浓溶液中分离得到纯净的NaCl |
16.向某无色溶液中加入铁粉能产生大量H2,则该溶液中可能含有的能大量共存的离子组是( )
| A. | Na+、Ca2+、Cl-、NO3- | B. | Fe3+、K+、Cl-、HCO3- | ||
| C. | Cu2+、Na+、Cl-、SO42- | D. | K+、Na+、Cl-、SO42- |
6.下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是( )
| A. | 高锰酸钾、硫酸铜、澄清石灰水 | B. | 水、空气、纯碱 | ||
| C. | 氧化铁、空气、熟石灰 | D. | 硝酸、食盐水、烧碱 |
13.伞形酮可由雷琐苯乙酮和苹果酸在一定条件下反应制得,下列说法错误的是( )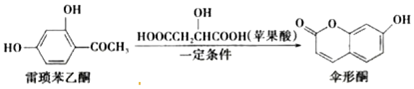

| A. | 雷琐苯乙酮有两种含氧官能团 | |
| B. | 1 mol伞形酮与足量 NaOH溶液反应,最多可消耗 2 mol NaOH | |
| C. | 伞形酮难溶于水 | |
| D. | 雷琐苯乙酮和伞形酮都能跟 FeCl3溶液发生显色反应 |
10.Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是( )
| A. | Na2CO3是钠盐 | B. | Na2CO3是含氧酸盐 | ||
| C. | Na2CO3是碳酸盐 | D. | Na2CO3是碱 |
11.下列实验操作及数据记录正确的是( )
| A. | 用量筒量取KMnO4溶液12.00mL | |
| B. | 测定中和热时将NaOH溶液迅速一次性倒入盛有盐酸的小烧杯中,盖好盖板 | |
| C. | 常温下,测得0.01mol/LNaHCO3溶液的pH值=12 | |
| D. | 加热蒸发FeCl3溶液,获得FeCl3固体 |