题目内容
1.工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾.为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO2转化为有用的副产品.请按要求回答下列问题: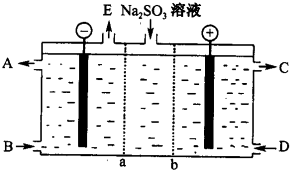
(1)硫酸工厂尾气中的SO2通常用足量石灰水吸收,然后再用稀硫酸处理.
①写出上述过程反应的化学方程式:SO2+Ca(OH)2=CaSO3↓+H2O、CaSO3+H2SO4=CaSO4+SO2↑+H2O.
②请说出这种尾气处理方法的优点(说出两点即可):原料生石灰,硫酸价格便宜且容易获得;可得副产品石膏或SO2可作为生产化肥的原料.
③生产中往往需要向溶液中加入适量的对苯二酚或对苯二胺等还原性物质,其目的是防止亚硫酸盐被氧化,不利于后期二氧化硫回收.
(2)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将所得的Na2SO3溶液进行电解循环再生,这种新工艺叫再生循环脱硫法;其中阴阳膜组合循环再生机理如图所示,a、b离子交换膜将电解槽分为三个区域,电极材料为石墨.
①图中a表示阳离子交换膜(填“阴”或“阳”).A~E分别代表生产中的原料或产品,其中C是硫酸,则A是NaOH溶液,E是氢气.
②阳极的电极反应式为SO32--2e-+H2O=2H++SO42-.
分析 1)①二氧化硫雨氢氧化钙反应生成亚硫酸钙,加入硫酸,可生成硫酸钙和二氧化硫气体;
②可从原料价廉易得,SO2回收利用角度分析;
③加入适量的对苯二酚或对苯二胺等还原性物质,可防止亚硫酸盐被氧化;
(2)①从C为硫酸可知,b为阴离子交换膜.故a为阳离子交换膜.在阴极区应为水放电生成氢气和氢氧根,故A为氢氧化钠,E为氢气;
②阳极应为亚硫酸根放电生成硫酸根.
解答 解:(1)①SO2与足量石灰水反应,生成亚硫酸钙和水,亚硫酸钙和硫酸反应生成硫酸钙、水和二氧化硫,发生的化学反应分别为SO2+Ca(OH)2=CaSO3↓+H2O、CaSO3+H2SO4=CaSO4+SO2↑+H2O,
故答案为:SO2+Ca(OH)2=CaSO3↓+H2O;CaSO3+H2SO4=CaSO4+SO2↑+H2O;
②这种尾气处理方法的优点有:原料生石灰、硫酸价格便宜且容易获得;可得到石膏副产品;产生的SO2含量较高可返回作为原料,
股答案为:原料生石灰,硫酸价格便宜且容易获得;可得副产品石膏或SO2可作为生产化肥的原料;
③加入适量的对苯二酚或对苯二胺等还原性物质,可防止亚硫酸盐被氧化,不利于后期二氧化硫回收,故答案为:防止亚硫酸盐被氧化,不利于后期二氧化硫回收;
(2)①从C为硫酸可知,硫酸根来源于亚硫酸根放电.故b为阴离子交换膜,a为阳离子交换膜,在阴极区应为水放电生成氢气和氢氧根离子,故A为氢氧化钠,E为氢气,
故答案为:阳;NaOH溶液;氢气;
②阳极应为亚硫酸根放电生成硫酸根,反应的离子方程式为SO32--2e-+H2O=2H++SO42-,故答案为:SO32--2e-+H2O=2H++SO42-.
点评 本题考查酸雨的防治以及二氧化硫的性质,为高频考点,侧重于学生的分析能力的考查,题目涉及化学与技术及工业生产的考查,有利于培养学生良好的科学素养,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案| A. | 漂白粉长期暴露在空气中最后会变质失效 | |
| B. | 对“地沟油”进行分馏可得到汽油 | |
| C. | PM2.5是对空气中直径小于或等于2.5微米(2.5×10-6m)的固体颗粒或液滴的总称,其分散在空气中一定形成气溶胶 | |
| D. | 氯气溶于水生成次氯酸有强氧化性,可以起净水和杀菌消毒的作用 |
| A. | 若电解熔融MgCl2产生1 mol Mg,理论上转移的电子数约为2×6.02×1023 | |
| B. | 海轮船体镶嵌锌块是牺牲阳极的阴极保护法,防止船体被腐蚀 | |
| C. | 室温下,pH均为3的盐酸和NH4Cl溶液中,水的电离程度相同 | |
| D. | 一定条件下反应2SO2+O2?2SO3达到平衡时,v正(O2)=2v逆(SO3) |
| A. | 稀硫酸中:K+、MnO4-、CH3CH2OH | |
| B. | pH=10的溶液中:Na+、SO32-、NH3•H2O | |
| C. | 中性溶液中:Na+、NO3-、AlO2- | |
| D. | FeCl3溶液中:H2O2、Mg2+、SO42- |
| A. | 放热的自发过程都是熵值减小的过程 | |
| B. | 吸热的自发过程常常是熵值增加的过程 | |
| C. | 水自发地从高处流向低处,是趋向能量最低状态的倾向 | |
| D. | 只根据焓变来判断化学反应的方向是可以的 |

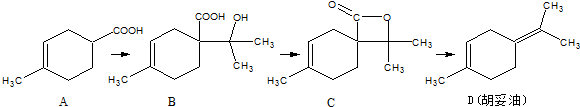
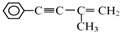 的反应条件是浓硫酸、加热.
的反应条件是浓硫酸、加热.
 或
或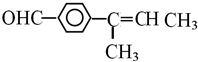 (任写一个)
(任写一个)