题目内容
14.设NA表示阿伏加德罗常数,下列说法不正确的是( )| A. | 2.7克金属铝变为铝离子时失去的电子数目为0.3NA | |
| B. | 标准状况,0.5molN2含有的分子数为0.5NA | |
| C. | 在常温、常压下,1molHCl、H2O或I2所含有的分子数都为 NA | |
| D. | 在同温、同压下,相同物质的量的任何气体单质所含有的原子数相同 |
分析 A、2.7g金属铝为0.1mol,铝反应中失去3个电子;
B.气体分子数=气体物质的量×NA;
C.气体分子数=气体物质的量×NA;
D.根据分子的组成判断,分子的组成原子数不一定相等,例如常见分子:O2、He、O3、CH4等.
解答 解:A、铝原子反应失去3个电子,2.7g铝为0.1mol,失去0.3mole-,失去的电子数目为0.3NA,故A正确;
B.气体分子数=气体物质的量×NA=0.5NA,故B正确;
C.在常温、常压下,1molHCl、H2O或I2所含有的分子数都为 1mol即为NA,故C正确;
D.分子的组成原子数不一定相等,例如常见分子:O2、He、O3、CH4等,在同温、同压下,相同物质的量的任何气体单质所含有的分子数相同,故D错误;
故选D.
点评 本题借助阿伏伽德罗常数,考查了有关气体摩尔体积、微粒数目和物质的量的计算,气体阿伏伽德罗定律的应用,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.表为各物质中所含的杂质以及除去这些杂质选用的试剂或操作方法,正确的是( )
| 物质 | 杂质 | 除杂试剂或操作方法 | |
| A. | CuSO4 | FeSO4 | 加入过量铁粉,过滤 |
| B. | NaNO3 | CaCO3 | 溶解、过滤、蒸发 |
| C. | NaCl溶液 | I2 | 加酒精,萃取分液 |
| D. | KNO3溶液 | AgNO3 | 加入NaCl溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
2.下列物质中,长期露置在空气中不会变质的是( )
| A. | AgI | B. | 漂白粉 | C. | 食盐 | D. | 次氯酸溶液 |
9.在盛有溴水的试管中,加入少量苯后振荡,静置后( )
| A. | 整个溶液变橙色 | B. | 整个溶液变浅棕色 | ||
| C. | 上层无色、下层橙色 | D. | 下层无色、上层橙色 |
19.萃取碘水中的碘,可用的萃取剂是( )
①四氯化碳 ②汽油 ③酒精 ④苯 ⑤甲苯.
①四氯化碳 ②汽油 ③酒精 ④苯 ⑤甲苯.
| A. | 只有① | B. | ①②④和⑤ | C. | ①和③ | D. | ①②③ |
6.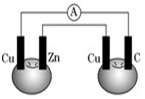 重庆市璧山中学校在化学兴趣活动中,曾老师利用番茄做成电池(如图所示),铜片和锌片用导线连接后插入番茄里,则碳是( )
重庆市璧山中学校在化学兴趣活动中,曾老师利用番茄做成电池(如图所示),铜片和锌片用导线连接后插入番茄里,则碳是( )
 重庆市璧山中学校在化学兴趣活动中,曾老师利用番茄做成电池(如图所示),铜片和锌片用导线连接后插入番茄里,则碳是( )
重庆市璧山中学校在化学兴趣活动中,曾老师利用番茄做成电池(如图所示),铜片和锌片用导线连接后插入番茄里,则碳是( )| A. | 阳极 | B. | 正极 | C. | 阴极 | D. | 负极 |
3.已知5KCl+KClO3+3H2SO4═3Cl2↑+3K2SO4+3H2O,下列说法不正确的是( )
| A. | H2SO4既不是氧化剂又不是还原剂 | |
| B. | 1molKClO3参加反应时有5mol电子转移 | |
| C. | KClO3是氧化剂 | |
| D. | 被氧化与被还原的氯元素的质量比为1:5 |
4.能把Na2SO4、NH4NO3、KCl、(NH4)2SO4四瓶溶液加以区别的一种试剂是( )
| A. | Ba(OH)2 | B. | BaCl2 | C. | Ba(NO3)2 | D. | NaOH |