题目内容
已知:化学反应3Ag+4HNO3(稀)═3AgNO3+NO↑+2H2O
(1)该反应的离子方程式为:
(2)当有32.4克银溶解时,反应生成的NO在标况下的体积是多少?
(3)当有0.2mol银溶解时,有多少克HNO3被还原?
(1)该反应的离子方程式为:
(2)当有32.4克银溶解时,反应生成的NO在标况下的体积是多少?
(3)当有0.2mol银溶解时,有多少克HNO3被还原?
考点:化学方程式的有关计算
专题:计算题
分析:(1)单质和气体、弱电解质写化学式,可溶性的强电解质写离子,据此书写离子方程式;
(2)根据银和一氧化氮之间的关系式计算;
(3)根据转移电子守恒计算被还原的硝酸.
(2)根据银和一氧化氮之间的关系式计算;
(3)根据转移电子守恒计算被还原的硝酸.
解答:
解:(1)单质和气体、弱电解质写化学式,可溶性的强电解质写离子,该反应离子方程式为:
3Ag+4H++NO3-═3Ag++NO↑+2H2O,
故答案为:3Ag+4H++NO3-═3Ag++NO↑+2H2O;
(2)设生成一氧化氮体积为x,
3Ag+4H++NO3-═3Ag++NO↑+2H2O
324g 22.4L
32.4g x
x=
=2.24L
答:生成NO的体积为2.24L;
(3)根据转移电子守恒得被还原的硝酸的物质的量=
=
,
被还原的硝酸的质量=
mol×63g/mol=4.2g,
答:被还原的硝酸的质量为4.2g.
3Ag+4H++NO3-═3Ag++NO↑+2H2O,
故答案为:3Ag+4H++NO3-═3Ag++NO↑+2H2O;
(2)设生成一氧化氮体积为x,
3Ag+4H++NO3-═3Ag++NO↑+2H2O
324g 22.4L
32.4g x
x=
| 32.4g×22.4L |
| 324g |
答:生成NO的体积为2.24L;
(3)根据转移电子守恒得被还原的硝酸的物质的量=
| 0.2mol×1 |
| 5-2 |
| 1 |
| 15mol |
被还原的硝酸的质量=
| 1 |
| 15 |
答:被还原的硝酸的质量为4.2g.
点评:本题考查了离子方程式的书写、氧化还原反应的有关计算,根据方程式中银和一氧化氮、被还原硝酸之间的关系式来分析解答即可,注意部分硝酸被还原,难度不大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A、标准状况下,22.4 L CO2和O2混合气体中含有的氧分子数约为NA |
| B、常温常压下,0.1 mol Fe在0.1 mol Cl2中充分燃烧,转移的电子数为0.2NA |
| C、标准状况下,11.2L NO与11.2L O2 混合后所含原子数为2NA |
| D、电解精炼铜时,电解池中每转移1mol电子,阳极上溶解的铜原子数为0.5 NA |
化学用语是表示物质组成、结构和变化规律的一种具有国际性、科学性和规范性的书面语言.下列化学用语中表述正确的是( )
A、次氯酸的电子式: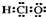 |
| B、二氧化硅的分子式:SiO2 |
C、二氧化碳的比例模型: |
D、Cl-的结构示意图: |
设阿伏加德罗常数的值为NA,下列说法正确的是( )
| A、1mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA |
| B、标准状况下,2.24L已烷含有原子的数目为2NA |
| C、1mol甲醇中含有C-H键的数目为4NA |
| D、11.2升氯气所含的原子数目一定为NA |
要除去CO2中混有的少量HCl气体,最好的方法是将气体通过( )
| A、饱和NaHCO3溶液 |
| B、Na2CO3溶液 |
| C、饱和石灰水 |
| D、烧碱溶液 |
 肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.