题目内容
(8分)已知反应N2O4(g)==2NO2(g) △H=57.24kJ·mol-1 △S=176J·mol-1·K-1则在298.15K时该反应自发向 进行(填“左”或“右”),在500K时反应自发向 进行。
【答案】
左 右
【解析】
试题分析:根据△G=△H-T·△S可知,如果△H=57.24kJ·mol-1 △S=176J·mol-1·K-1则在298.15K时,△G=57.24-298×0.176=4.792>0,所以该反应自发向左进行;在500K时,△G=57.24-500×0.176=-30.76<0,所以该反应自发向右进行。
考点:考查△G的有关计算和反应自发性的有关判断
点评:本题是基础性试题的考查,难度不大,主要是训练学生的答题能力,以及灵活运用知识解决实际问题的能力,提高学习效率。

练习册系列答案
相关题目
下列常见分子中σ键、π键判断正确的是( )
| A、CN-与N2结构相似,CH2=CHCN分子中σ键与π键数目之比为1:1 | ||||||
| B、CO与N2结构相似,CO分子中σ键与π键数目之比为2:1 | ||||||
C、
| ||||||
| D、已知反应N2O4(l)+2N2H4(l)═3N2(g)+4H2O(l),若该反应中有4 mol N-H键断裂,则形成的π键数目为6NA |
已知可逆反应N2O4(g) 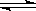 2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
| A.由于K2>K1,所以a>b |
| B.由于K随温度升高而增大,所以此反应的△H>0 |
| C.由于K随温度升高而增大,所以此反应的△H<0 |
| D.其它条件不变时,将盛有该混合气体的容器置于热水中,体系颜色变浅 |