题目内容
11.将pH=8的氢氧化钠溶液和pH=10的氢氧化钠溶液等体积混合后,溶液中的C(H+)最接近( )| A. | $\frac{{{{10}^{-8}}+{{10}^{-10}}}}{2}mol/L$ | B. | $\frac{{{{10}^{-6}}+{{10}^{-4}}}}{2}mol/L$ | ||
| C. | (10-8+10-10)mol/L | D. | 2×10-10mol/L |
分析 两种碱溶液混合,先计算出混合后溶液的c(OH-),再根据溶液中水的离子积计算出溶液的c(H+),据此分析解答.
解答 解:pH=8的NaOH溶液中c(OH-)=$\frac{1×1{0}^{-14}}{1×1{0}^{-8}}$=1×10-6mol/L,pH=10的NaOH溶液中c(OH-)=$\frac{1×1{0}^{-14}}{1×1{0}^{-10}}$=1×10-4mol/L,
混合液中氢氧根离子的浓度为:c(OH-)=$\frac{1{0}^{-6}+1{0}^{-4}}{2}$mol/L≈5×10-5mol/L,
则溶液中的c(H+)=$\frac{1×1{0}^{-14}}{5×1{0}^{-5}}$mol/L=2.0×10-10mol/L,
故选D.
点评 本题考查两种碱溶液混合后的溶液氢离子浓度计算,题目难度中等,注意先计算溶液中c(OH-),再计算c(H+),为易错点,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
1.电子表和电子计算器的电源通常用微型银-锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,电极总反应为:Ag2O+H2O+Zn=Zn(OH)2+2Ag.下列叙述正确的是( )
| A. | Zn是正极,Ag2O是负极 | |
| B. | Zn是负极,Ag2O是正极 | |
| C. | 工作时负极区溶液的pH增大 | |
| D. | 工作时电子由Ag2O极经外电路流向Zn极 |
2.由C5H10、C3H6O2和C6H12O6组成的混合物,经测定含氧元素的质量分数为x,则此混合物中含碳元素的质量分数为( )
| A. | $\frac{6(1-x)}{7}$ | B. | $\frac{1-x}{7}$ | C. | $\frac{3x}{4}$ | D. | 无法计算 |
6.NA表示阿伏加德罗常数的值.下列说法中正确的是( )
| A. | 常温常压下,16g O3所含的原子数为NA | |
| B. | 标准状况下,11.2 L NO和11.2 L O2混合后气体的分子总数为NA | |
| C. | 常温下,pH=2的稀盐酸中所含有的H+离子数等于0.01 NA | |
| D. | 加热条件下,20mL 10 mol/L 浓硝酸与足量铜反应转移电子数等于0.2NA |
16.对SO2与SO3说法正确的是( )
| A. | 都是直线形结构 | |
| B. | 中心原子都采取sp3杂化轨道 | |
| C. | SO2中S原子和SO3中S原子上都没有孤对电子 | |
| D. | SO2为V形结构,SO3为平面三角形结构 |
3.下列化合物中,既能发生水解反应,又能发生消去反应,且消去反应生成的烯烃不存在同分异构体的是( )
| A. | CH3Cl | B. | 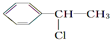 | C. | 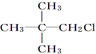 | D. | 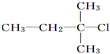 |
20.下列说法错误的是( )
| A. | 原子及其简单阴离子的核外电子层数都等于该元素所在的周期数 | |
| B. | 原子最外层电子数都等于其所在的族序数 | |
| C. | 元素周期表从ⅢB到ⅡB族共8个纵行,全都是金属元素 | |
| D. | 同周期表中ⅦA族元素的原子半径较小 |
3.下列叙述正确的是( )
| A. | 漂白粉、次氯酸溶液和明矾都是混合物 | |
| B. | 不能通过化合反应制得FeCl2和Fe(OH)3 | |
| C. | 铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧 | |
| D. | 用强光照射装满次氯酸的试管(倒置于水槽中)可收集到两种气体 |

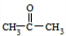 +2H2O;
+2H2O;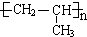 .
.