题目内容
在含Mg2+的溶液里,c(Cl-)为0.15 mol/L、c(![]() )为0.025 mol/L、c(Na+)为0.05 mol/L.取100 mL该溶液,向其中加入NaOH固体使Mg2+完全沉淀,所加NaOH的物质的量至少为________.
)为0.025 mol/L、c(Na+)为0.05 mol/L.取100 mL该溶液,向其中加入NaOH固体使Mg2+完全沉淀,所加NaOH的物质的量至少为________.
答案:0.015mol
解析:
提示:
解析:
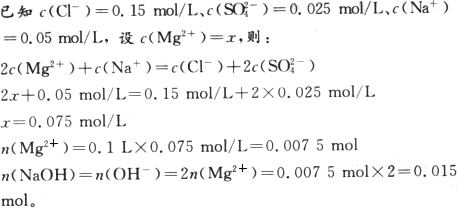
提示:
在电解质溶液里,阴、阳离子所带电荷的定量关系是:
正电荷总数=负电荷总数
或正电荷总物质的量=负电荷总物质的量
或正电荷总浓度(mol/L)=负电荷总浓度(mol/L)

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
