题目内容
实验室用二氧化锰和浓盐酸反应制氯气.现将8.7g的二氧化锰与50ml 12mol?L-1的浓盐酸共热:
(1)当有0.10mol电子发生转移时,能生成标准状况下的氯气 L.
(2)完全反应后被氧化的HCl的质量为 g.
(3)若向完全反应后的溶液中加入足量的AgNO3溶液,能产生白色沉淀 mol.
(1)当有0.10mol电子发生转移时,能生成标准状况下的氯气
(2)完全反应后被氧化的HCl的质量为
(3)若向完全反应后的溶液中加入足量的AgNO3溶液,能产生白色沉淀
考点:化学方程式的有关计算
专题:计算题
分析:(1)根据电子转移守恒计算氯气的物质的量,再根据V=nVm计算氯气的体积;
(2)被氧化的HCl生成氯气,根据氯原子守恒计算被氧化HCl的物质的量,再根据m=nM计算;
(3)根据氯元素守恒计算反应后溶液中n(Cl-),而n(AgCl)=n(Cl-).
(2)被氧化的HCl生成氯气,根据氯原子守恒计算被氧化HCl的物质的量,再根据m=nM计算;
(3)根据氯元素守恒计算反应后溶液中n(Cl-),而n(AgCl)=n(Cl-).
解答:
解:(1)根据电子转移守恒,生成氯气的物质的量=
=0.05mol,标况下,生成氯气的体积=0.05mol×22.4L/mol=1.12L,故答案为:1.12;
(2)被氧化的HCl生成氯气,根据氯原子守恒,被氧化HCl的物质的量=0.05mol×2=0.1mol,则被氧化HCl的质量=0.1mol×36.5g/mol=3.65g,故答案为:3.65;
(3)根据氯元素守恒,反应后溶液中n(Cl-)=0.05L×12mol/L-0.05mol×2=0.5mol,而n(AgCl)=n(Cl-)=0.5mol,故答案为:0.5.
| 0.1mol |
| 2 |
(2)被氧化的HCl生成氯气,根据氯原子守恒,被氧化HCl的物质的量=0.05mol×2=0.1mol,则被氧化HCl的质量=0.1mol×36.5g/mol=3.65g,故答案为:3.65;
(3)根据氯元素守恒,反应后溶液中n(Cl-)=0.05L×12mol/L-0.05mol×2=0.5mol,而n(AgCl)=n(Cl-)=0.5mol,故答案为:0.5.
点评:本题考查氧化还原反应有关计算,比较基础,注意利用守恒思想解答.

练习册系列答案
相关题目
已知碱能除去硝酸工业废气中的NO2和NO:NO2+NO+2NaOH═2NaNO2+H2O;2NO2+2NaOH═NaNO2+NaNO3+H2O.根据上述反应原理,下列气体中不能被过量的NaOH吸收的是( )
| A、1mol O2和4mol NO2 |
| B、1mol NO和4mol NO2 |
| C、1mol O2和4mol NO |
| D、1mol NO2和4mol NO |
下列化学用语使用正确的是( )
A、氟化镁的电子式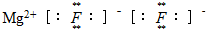 |
B、用电子式表示硫化氢的形成过程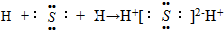 |
| C、HClO的结构式 H-O-Cl |
D、Cl-离子的结构示意图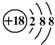 |
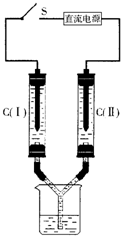 如图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极.接通S后,C(Ⅱ)附近溶液变红,两玻璃管中有气体生成.下列说法正确的是( )
如图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极.接通S后,C(Ⅱ)附近溶液变红,两玻璃管中有气体生成.下列说法正确的是( )| A、C(Ⅰ)电极产生可燃性气体 | ||||
| B、C(Ⅱ)的电极附近溶液呈碱性 | ||||
| C、C(Ⅱ) 电极产生的气体可使湿润的碘化钾淀粉试纸变蓝色 | ||||
D、电解过程中发生的化学方程式为:2NaCl
|
下列说法正确的是( )
| A、在标准状况下,1摩尔任何物质的体积都约为22.4升 |
| B、22.4升氧气所含的氧原子数为2 NA个 |
| C、在标准状况下,1摩尔水的体积约为22.4升 |
| D、1摩尔某气体的体积约为22.4升时,该气体不一定处于标准状况下 |
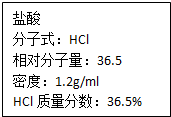 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题: