题目内容
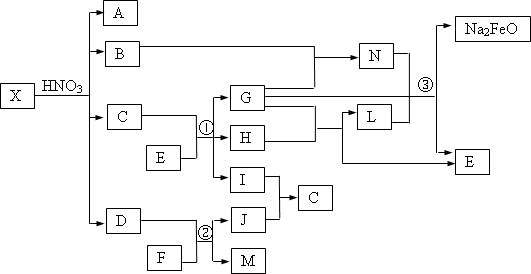
A通常存在于钢铁中,它是由甲、乙两种化合物组成的混合物,甲和乙的含量、形状、分布对钢性能影响很大,使钢硬而脆,不宜进行机械加工。已知:(1)甲和乙的组成元素相同,均是由两种常见元素的原子以最简整数比构成的化合物,其相对分子质量分别为124、180。(2)C、D、H、I、J常温下为气体,H、I、J为单质,D是一种红棕色气体。(3)反应②为制备理想的绿色水处理剂Na2FeO4(高铁酸钠)的一种方法(图中部分生成物没有列出)。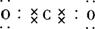
请填写以下空白:
(1)写出C的电子式________________。
(2)写出反应①的化学方程式________________。
反应②的离子方程式________________。
(3)甲和乙的化学式分别为________________、________________,若A中组成元素的物质的量之比为4:9,则乙在A中的物质的量分数为________________。
(1) ![]()
(2)4NO2+O2+2H2O![]() 4HNO3
4HNO3
2Fe(OH)3+3ClO-+4OH-![]()
![]() +3Cl-+5H2O
+3Cl-+5H2O
(3)Fe
【解析】钢的主要成分是Fe(56),除此之外,通常还含有合金元素硅(28)、锰(55)及杂质成分硫(32)和磷(31)等,甲和乙相对分子质量的差值为180-124=56,初步分析,甲和乙在组成上可能是相差1个Fe原子或相差2个Si原子。根据“D是一种红棕色气体”可知,D是NO2。根据转化图中的反应“C(气体)+Na2O![]() G
G![]() 4HNO3。根据“E(H2O)+L
4HNO3。根据“E(H2O)+L![]() I(单质,气体)+J(单质,气体)+K”和“J(单质,气体)+K
I(单质,气体)+J(单质,气体)+K”和“J(单质,气体)+K![]() L+M”,联想氯碱工业(电解饱和食盐水)及Cl2与NaOH溶液的反应,进行验证,完全符合,即L是NaCl,I是H2,J是Cl2,K是KOH,M是NaClO。反应②的化学方程式为2Fe(OH)3+3NaClO+4NaOH
L+M”,联想氯碱工业(电解饱和食盐水)及Cl2与NaOH溶液的反应,进行验证,完全符合,即L是NaCl,I是H2,J是Cl2,K是KOH,M是NaClO。反应②的化学方程式为2Fe(OH)3+3NaClO+4NaOH ![]() 2Na2FeO4+3NaCl+5H2O,相应的离子方程式为2Fe(OH)3+3ClO-+4OH-
2Na2FeO4+3NaCl+5H2O,相应的离子方程式为2Fe(OH)3+3ClO-+4OH-![]()
![]() +3Cl-+5H2O。
+3Cl-+5H2O。
(3)设A物质中Fe![]() ,得出
,得出![]() =3,即A物质中Fe
=3,即A物质中Fe

| |||||||||||||||