题目内容
煤经过化学加工可转化为气体或液体以及各种化工产品,从而提高了煤的利用率.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:
C(s)+H2O(g)?CO(g)+H2(g)△H=+131.5kJ?mol-1
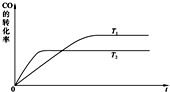
①下列措施中,能提高碳的转化率的是 (填字母序号)
a.容器的体积不变,增加水蒸气的物质的量
b.缩小容器的体积,增大压强
c.及时将水煤气从容器中移走
d.其他条件不变,升高温度
②又知C(s)+CO2 (g)?2CO(g)△H=+172.5kJ?mol-1则CO(g)+H2O(g)?CO2(g)+H2(g)的焓变(△H)为 .
(2)CO和H2在一定条件下可反应生成甲醇,CO(g)+2H2(g)?CH3OH(g).甲醇是一种燃料,可用于设计燃料电池.如图是甲醇燃料电池的原理示意图.
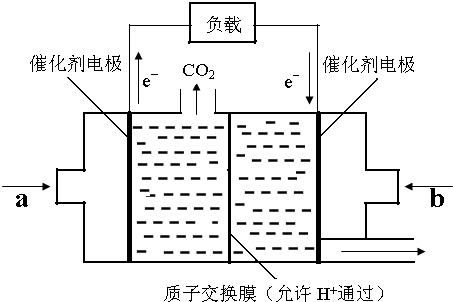
①a处通入的是 (填物质名称),右侧电极上发生 (填“氧化”或“还原”)反应.
②该电池工作过程中,H+的移动方向为从 到 (填“左”或“右”).
③该电池负极反应式为 .
④若用该电池提供的电能电解600ml 0.2mol?L-1NaCl溶液,设有0.01mol CH3OH完全放电,且电解产生的Cl2全部溢出,电解前后忽略溶液体积的变化,则电解时阳极反应式为 ,电解结束后所得溶液的pH= .若向电解后的溶液加入适量的醋酸至溶液的pH恰好等于7(反应前后忽略溶液体积的变化),则此时溶液中c(Na+):c(CH3COO-)= .
(3)在25℃时,将两个铂电极插入一定量的硫酸钠饱和溶液中进行电解,通电一段时间后,阴极逸出a mol气体,同时有W g Na2SO4?10H2O晶体析出,若温度不变,此时剩余溶液的质量分数是 (用含字母a、W的代数式表示).
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:
C(s)+H2O(g)?CO(g)+H2(g)△H=+131.5kJ?mol-1
①下列措施中,能提高碳的转化率的是
a.容器的体积不变,增加水蒸气的物质的量
b.缩小容器的体积,增大压强
c.及时将水煤气从容器中移走
d.其他条件不变,升高温度
②又知C(s)+CO2 (g)?2CO(g)△H=+172.5kJ?mol-1则CO(g)+H2O(g)?CO2(g)+H2(g)的焓变(△H)为
(2)CO和H2在一定条件下可反应生成甲醇,CO(g)+2H2(g)?CH3OH(g).甲醇是一种燃料,可用于设计燃料电池.如图是甲醇燃料电池的原理示意图.

①a处通入的是
②该电池工作过程中,H+的移动方向为从
③该电池负极反应式为
④若用该电池提供的电能电解600ml 0.2mol?L-1NaCl溶液,设有0.01mol CH3OH完全放电,且电解产生的Cl2全部溢出,电解前后忽略溶液体积的变化,则电解时阳极反应式为
(3)在25℃时,将两个铂电极插入一定量的硫酸钠饱和溶液中进行电解,通电一段时间后,阴极逸出a mol气体,同时有W g Na2SO4?10H2O晶体析出,若温度不变,此时剩余溶液的质量分数是
考点:化学平衡的影响因素,热化学方程式,电极反应和电池反应方程式
专题:
分析:(1)①根据平衡的移动判断.
②根据盖斯定律计算.
(2)①电池总反应为:2CH3OH+3O2=2CO2+4H2O,原电池中电子从负极经外电路流向正极,由图可知,左侧电极流出电子,为负极,发生氧化反应,所以,a处通入甲醇.
②甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路通过质子交换膜到达另一极与氧气反应.
③H+与氧气在正极发生还原反应.
④计算出0.01molCH3OH完全放电转移的电子的物质的量,根据电解氯化钠溶液原理,可知电解生成氢氧化钠为电解过程转移的电子的物质的量,利用Kw求出H+浓度,再利用pH=-logc(H+)计算,分析电解后溶液中离子物质的量和溶液中电荷守恒计算得到;
(3)用Pt作电极,电解饱和硫酸钠溶液时,阳极上氢氧根离子放电生成氧气,阴极上氢离子放电生成氢气,实际上是电解的水,发生总反应2H2O
O2↑+2H2↑,电解水后,溶液中硫酸钠过饱和导致析出晶体,剩余的电解质溶液仍是饱和溶液,析出的硫酸钠晶体和电解的水组成的也是饱和溶液,根据质量分数公式计算即可.
②根据盖斯定律计算.
(2)①电池总反应为:2CH3OH+3O2=2CO2+4H2O,原电池中电子从负极经外电路流向正极,由图可知,左侧电极流出电子,为负极,发生氧化反应,所以,a处通入甲醇.
②甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路通过质子交换膜到达另一极与氧气反应.
③H+与氧气在正极发生还原反应.
④计算出0.01molCH3OH完全放电转移的电子的物质的量,根据电解氯化钠溶液原理,可知电解生成氢氧化钠为电解过程转移的电子的物质的量,利用Kw求出H+浓度,再利用pH=-logc(H+)计算,分析电解后溶液中离子物质的量和溶液中电荷守恒计算得到;
(3)用Pt作电极,电解饱和硫酸钠溶液时,阳极上氢氧根离子放电生成氧气,阴极上氢离子放电生成氢气,实际上是电解的水,发生总反应2H2O
| ||
解答:
解:(1)①a、容器的容积不变,增加水蒸汽的物质的量,水蒸汽的浓度增大,平衡向正反应移动,碳的转化率提高,故a正确;
b、缩小容器的容积,增大压强,平衡向体积减小的方向移动,即向逆反应移动,碳的转化率降低,故b错误;
c、及时将水煤气从容器中移走,生成物的浓度降低,平衡向正反应移动,碳的转化率提高,故c正确;
d、该反应为吸热反应,其他条件不变,升高温度,向吸热方向移动,即平衡向正反应移动,碳的转化率提高,故d正确;
故答案为:acd;
②已知反应:①C(s)+H2O(g)?CO(g)+H2(g);△H=131.5kJ?mol-1
②C(s)+CO2(g)?2CO(g);△H=172.5kJ?mol-1
所以①-②得,CO(g)+H2O(g)?CO2(g)+H2(g);△H=-41kJ?mol-1
故答案为:-41kJ?mol-1
(2))①电池总反应为:2CH3OH+3O2=2CO2+4H2O,原电池中电子从负极经外电路流向正极,由图可知,左侧电极流出电子,为负极,发生氧化反应,右侧发生还原反应,所以,a处通入甲醇,
故答案为:甲醇;还原;
②甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路通过质子交换膜到达另一极与氧气反应.所以H+的移动方向为从左到右.
故答案为:左;右;
③H+与氧气在正极发生还原反应,电极反应式为4H++O2+4e-=2H2O,甲醇在负极反应,电极反应式为:CH3OH-6e-+H2O=CO2+6H+,
故答案为:CH3OH-6e-+H2O=CO2+6H+;
④0.01molCH3OH完全放电转移的电子的物质的量为0.01mol×[4-(-2)]=0.06mol,根据电解氯化钠溶液原理,阳极反应式为2 Cl--2e-=Cl2↑;正极反应式为:2H++2e-=H2↑或2H2O+2e-=H2↑+2OH-,可知溶液中n(OH-)=0.06mol,所以c(OH-)=
=0.1mol/L,所以c(H+)
=
=10-13,pH=-logc(H+)=-log(10-13)=13;电解后溶液中氯化钠中氯离子剩余0.6L×0.2mol?L-1-0.06mol=0.06mol,钠离子剩余0.12mol,若向电解后的溶液加入适量的醋酸至溶液的pH恰好等于7,溶液中溶质为CH3COOH和CH3COONa,溶液中存在电荷守恒,c(Na+)+c(H+)=c(OH-)+c(CH3COO-)+c(Cl-),c(Na+)=c(CH3COO-)+c(Cl-),c(Na+):c(CH3COO-)=2:1;
故答案为:2 Cl--2e-=Cl2↑;13;2:1;
(3)用Pt作电极,电解饱和硫酸钠溶液时,阳极上氢氧根离子放电生成氧气,阴极上氢离子放电生成氢气,电解水后,溶液中硫酸钠过饱和导致析出晶体,剩余的电解质溶液仍是饱和溶液,析出的硫酸钠晶体和电解的水组成的也是饱和溶液,
w g Na2SO4?10H2O硫酸钠的质量=w g×
=
g,
设电解水的质量为x:
2H2O
O2↑+2H2↑,
36g 2mol
x amol
x=18ag
所以饱和溶液的质量分数=
×100%=
%,故答案为:
%.
b、缩小容器的容积,增大压强,平衡向体积减小的方向移动,即向逆反应移动,碳的转化率降低,故b错误;
c、及时将水煤气从容器中移走,生成物的浓度降低,平衡向正反应移动,碳的转化率提高,故c正确;
d、该反应为吸热反应,其他条件不变,升高温度,向吸热方向移动,即平衡向正反应移动,碳的转化率提高,故d正确;
故答案为:acd;
②已知反应:①C(s)+H2O(g)?CO(g)+H2(g);△H=131.5kJ?mol-1
②C(s)+CO2(g)?2CO(g);△H=172.5kJ?mol-1
所以①-②得,CO(g)+H2O(g)?CO2(g)+H2(g);△H=-41kJ?mol-1
故答案为:-41kJ?mol-1
(2))①电池总反应为:2CH3OH+3O2=2CO2+4H2O,原电池中电子从负极经外电路流向正极,由图可知,左侧电极流出电子,为负极,发生氧化反应,右侧发生还原反应,所以,a处通入甲醇,
故答案为:甲醇;还原;
②甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路通过质子交换膜到达另一极与氧气反应.所以H+的移动方向为从左到右.
故答案为:左;右;
③H+与氧气在正极发生还原反应,电极反应式为4H++O2+4e-=2H2O,甲醇在负极反应,电极反应式为:CH3OH-6e-+H2O=CO2+6H+,
故答案为:CH3OH-6e-+H2O=CO2+6H+;
④0.01molCH3OH完全放电转移的电子的物质的量为0.01mol×[4-(-2)]=0.06mol,根据电解氯化钠溶液原理,阳极反应式为2 Cl--2e-=Cl2↑;正极反应式为:2H++2e-=H2↑或2H2O+2e-=H2↑+2OH-,可知溶液中n(OH-)=0.06mol,所以c(OH-)=
| 0.06mol |
| 0.6L |
| KW |
| c(OH-) |
| 10-14 |
| 0.1 |
故答案为:2 Cl--2e-=Cl2↑;13;2:1;
(3)用Pt作电极,电解饱和硫酸钠溶液时,阳极上氢氧根离子放电生成氧气,阴极上氢离子放电生成氢气,电解水后,溶液中硫酸钠过饱和导致析出晶体,剩余的电解质溶液仍是饱和溶液,析出的硫酸钠晶体和电解的水组成的也是饱和溶液,
w g Na2SO4?10H2O硫酸钠的质量=w g×
| 142 |
| 322 |
| 71W |
| 161 |
设电解水的质量为x:
2H2O
| ||
36g 2mol
x amol
x=18ag
所以饱和溶液的质量分数=
| ||
| (W+18a)g |
| 7100W |
| 161(W+18a) |
| 7100W |
| 161(W+18a) |
点评:本题综合性较大,涉及反应热、化学平衡、原电池、电解、pH值计算等,题目难度中等,注意利用盖斯定律计算反应热.

练习册系列答案
相关题目
浓盐酸与次氯酸钙能发生反应Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质是( )
①CO2 ②HCl ③H2O(g) ④O2.
①CO2 ②HCl ③H2O(g) ④O2.
| A、①②③④ | B、②③④ |
| C、②③ | D、①④ |
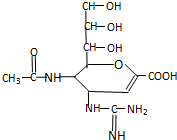 已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性.其分子结构如图:下列说法正确的是( )
已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性.其分子结构如图:下列说法正确的是( )| A、该物质的分子式为C12H19N4O7 |
| B、在一定条件下,该物质可以发生消去、加成、取代等反应 |
| C、1mol该物质与NaOH溶液反应,可以消耗4molNaOH |
| D、该物质能使溴水或高锰酸钾溶液褪色,能与FeCl3溶液发生显色反应 |
在锌与盐酸的反应中,HCl( )
| A、发生氧化反应 | B、是还原剂 |
| C、是氧化剂 | D、表现还原性 |


 煤间接液化是煤化工的一种重要方法:首先将原料煤与氧气、水蒸汽反应将煤全部气化,制得的粗煤气经变换、脱硫、脱碳制成洁净的合成气(CO+H2),然后合成气在催化剂作用下发生合成反应生成烃类,如:[nCO+(2n+1)H2=CnH2n+2+nH2O];或者合成醇类,如合成甲醇:CO(g)+2H2(g)?CH3OH(g).等等.
煤间接液化是煤化工的一种重要方法:首先将原料煤与氧气、水蒸汽反应将煤全部气化,制得的粗煤气经变换、脱硫、脱碳制成洁净的合成气(CO+H2),然后合成气在催化剂作用下发生合成反应生成烃类,如:[nCO+(2n+1)H2=CnH2n+2+nH2O];或者合成醇类,如合成甲醇:CO(g)+2H2(g)?CH3OH(g).等等. A、B、C是中学化学中常见的单质,常温下甲、乙两种化合物分别是黑色固体和无色液体,这些化合物和单质之间有如图所示关系.据此判断:
A、B、C是中学化学中常见的单质,常温下甲、乙两种化合物分别是黑色固体和无色液体,这些化合物和单质之间有如图所示关系.据此判断: