题目内容
(共14分)
Ⅰ.(2分)下列有关仪器的使用,能实现的是_______________(填序号)
A.用托盘天平称取11.70g食盐
B.用量筒量取12.36mL盐酸
C.用酸式滴定管量取21.20mL 0.10mol/L H2SO4溶液
D.用200mL容量瓶配制500mL 0.1mol/L NaCl溶液
Ⅱ.(6分)现用物质的量浓度为a mol/L的标准盐酸去测定V mL NaOH溶液的物质的量浓度,请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,还应该进行的操作是_______________________。
(2)下图是酸式滴定管中液面在滴定前后的读数:

C (NaOH) = _________________。
(3)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度会偏_________________。
III. (6分)我们知道空气中含有N2、O2、CO2、H2S等气体。试判断下列滴定操作的终点、分析下列现象的原因,并写出有关离子方程式。
(1)以酚酞为指示剂,用碱液滴定酸液到 为终点。约半分钟后导致褪色的原因: 。
(2)以淀粉为指示剂,用Na2S2O3滴定I2(2S2O32-+I2=S4O62-+2I-)到 为终点,约5min后溶液又显色的原因: 。
Ⅰ.(2分) C.
Ⅱ.(6分)(1)用已知物质的量浓度的标准盐酸润洗2到3次
(2)c (NaOH) = (V2-V1)a/V mol/L。
(3)高 (各2分)
III(6分)(1) 显现浅红色且在半分钟内不褪色;(1分) 空气中存在CO2 、H2S , CO2+OH-==HCO3-, H2S+OH-==HS-+H2O(2分,叙述合理即可,下同)
(2) 蓝色恰好褪去;(1分) 空气中存在O2; O2+4I-+4H+===2H2O+I2(2分)

 名校课堂系列答案
名校课堂系列答案

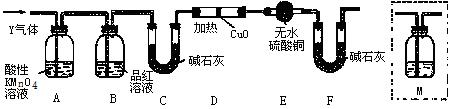
 ,需在装置中添加M于 (选填序号)。
,需在装置中添加M于 (选填序号)。