题目内容
17.将0.2mol/LCH3COOK与0.1mol/L盐酸等体积混合后,溶液中下列微粒的物质的量浓度的关系正确的是( )| A. | c(CH3COO-)=c(Cl-)=c(H+)>c(CH3COOH) | B. | c(CH3COO-)=c(Cl-)>c(CH3COOH)>c(H+) | ||
| C. | c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) | D. | c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
分析 将0.2mol/LCH3COOK与0.1mol/L盐酸等体积混合后,溶液中溶质为等物质的量浓度的CH3COOH、CH3COOK、KCl,CH3COOH电离程度大于CH3COO-水解程度导致混合溶液呈酸性,结合物料守恒判断.
解答 解:将0.2mol/LCH3COOK与0.1mol/L盐酸等体积混合后,溶液中溶质为等物质的量浓度的CH3COOH、CH3COOK、KCl,CH3COOH电离程度大于CH3COO-水解程度导致混合溶液呈酸性,
但CH3COOH的电离程度较小,结合物料守恒得c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+),故选D.
点评 本题考查离子浓度大小比较,为高频考点,明确混合溶液中溶质及其性质、溶液酸碱性是解本题关键,注意物料守恒的应用及弱电解质电离特点,题目难度不大.

练习册系列答案
相关题目
11.火箭推进器常以联氨(N2H4) 为燃料、过氧化氢为助燃剂.已知下列各物质反应的热化学方程式:N2H4(g)+O2(g)═N2(g)+2H2O(g)△H1=-533.23kJ•mol-1
H2O(g)═H2O (l)△H2=-44kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g)△H3=-196.4kJ•mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
H2O(g)═H2O (l)△H2=-44kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g)△H3=-196.4kJ•mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
| A. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=+817.63 kJ•mol-1 | |
| B. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ•mol-1 | |
| C. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=-641.63 kJ•mol-1 | |
| D. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-817.63 kJ•mol-1 |
8.下列说法正确的是( )
| A. | 铝在空气中耐腐蚀,所以铝是不活泼金属 | |
| B. | 铝能与冷水反应 | |
| C. | 铝热反应常用于冶炼某些熔点较高的金属 | |
| D. | 冶炼铝可用电解AlCl3的方法 |
12.(1)现有可逆反应.2NO2(g)═N2O4(g),△H<0,试根据图象判断t2、t3、t4时刻采取的措施.
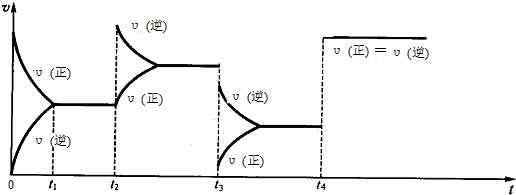
t2:增大生成物N2O4的浓度;t3:降低压强;t4:加入催化剂.
在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如表数据:
(2)40s时,NO2的产率是50%.
(3)20s时,N2O4的浓度为0.14mol/L,0~20s内N2O4的平均反应速率为0.003mol/(L.s).
(4)在80℃时该反应的平衡常数K值为0.54(保留2位小数).
(5)在其他条件相同时,该反应的K值越大,表明建立平衡时ABD.
A、N2O4的转化率越高 B、NO2的产量越大
C、N2O4与NO2的浓度之比越大 D、正反应进行的程度越大
(6)利用甲烷催化还原NOx:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ/mol
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为:CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g)△H=-867 kJ/mol.

t2:增大生成物N2O4的浓度;t3:降低压强;t4:加入催化剂.
在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如表数据:
| 时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0.20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(3)20s时,N2O4的浓度为0.14mol/L,0~20s内N2O4的平均反应速率为0.003mol/(L.s).
(4)在80℃时该反应的平衡常数K值为0.54(保留2位小数).
(5)在其他条件相同时,该反应的K值越大,表明建立平衡时ABD.
A、N2O4的转化率越高 B、NO2的产量越大
C、N2O4与NO2的浓度之比越大 D、正反应进行的程度越大
(6)利用甲烷催化还原NOx:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ/mol
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为:CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g)△H=-867 kJ/mol.
9.下列选项中,为完成相应实验,所用仪器、试剂及相关操作合理的是( )
| A. | 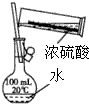 稀释浓硫酸 | |
| B. | 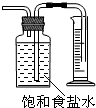 测量Cl2的体积 | |
| C. | 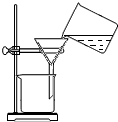 过滤 | |
| D. | 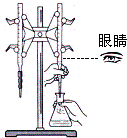 用NaOH标准溶液滴定锥形瓶中的盐酸 |
7.铝在人体中积累可使人慢性中毒,铝在下列使用场合须加以控制的是:①制炊具 ②制易拉罐 ③制电线电缆 ④煎制油条时使用明矾 ⑤用明矾净水( )
| A. | ①②④⑤ | B. | 仅②⑤ | C. | 仅②④⑤ | D. | ③④⑤ |