题目内容
相同温度、相同浓度下的六种电解质溶液,其pH由小到大的顺序如图所示,图中:①②③代表的物质可能分别为( )
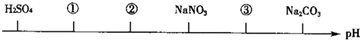
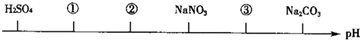
| A、NH4Cl;(NH4)2SO4;CH3COONa |
| B、(NH4)2SO4;NH4Cl;CH3COONa |
| C、(NH4)2SO4;NH4Cl;NaOH |
| D、CH3COOH;NH4Cl;(NH4)2SO4 |
考点:盐类水解的原理
专题:
分析:硫酸是强酸,其溶液呈酸性,硝酸钠是强酸强碱盐,其溶液呈中性,碳酸钠是强碱弱酸盐,其溶液呈碱性,根据图知,①②溶液呈酸性,且①的酸性大于②,则如果都是酸时,①中酸的电离程度大于②,如果都是强酸弱碱盐时,①的水解程度大于②的,如果是酸和盐时,则①是酸,②是盐,③溶液呈碱性,应该为盐溶液,且酸根离子的水解程度小于碳酸根离子.
解答:
解:硫酸是强酸,其溶液呈酸性,硝酸钠是强酸强碱盐,其溶液呈中性,碳酸钠是强碱弱酸盐,其溶液呈碱性,根据图知,①②溶液呈酸性,且①的酸性大于②,则如果都是酸时,①中酸的电离程度大于②,如果都是强酸弱碱盐时,①的水解程度大于②的,如果是酸和盐时,则①是酸,②是盐,③溶液呈碱性,应该为盐溶液,且酸根离子的水解程度小于碳酸根离子.
A.NH4Cl中铵根离子的浓度小于(NH4)2SO4的,水解程度小,酸性弱,故A错误;
B.(NH4)2SO4中铵根离子的浓度小于NH4Cl的,水解程度大,酸性强,所以符合图象,故B正确;
C.氢氧化钠是强碱,其碱性强于碳酸钠溶液的,故C错误;
D.(NH4)2SO4是强酸弱碱盐,其溶液呈酸性,故D错误;
故选B.
A.NH4Cl中铵根离子的浓度小于(NH4)2SO4的,水解程度小,酸性弱,故A错误;
B.(NH4)2SO4中铵根离子的浓度小于NH4Cl的,水解程度大,酸性强,所以符合图象,故B正确;
C.氢氧化钠是强碱,其碱性强于碳酸钠溶液的,故C错误;
D.(NH4)2SO4是强酸弱碱盐,其溶液呈酸性,故D错误;
故选B.
点评:本题考查了弱电解质的电离、盐类的水解等知识点,明确等浓度时,酸的强弱与溶液pH的关系、盐类水解程度与溶液pH的关系是解本题关键,难度中等.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
Na2O2可发生反应:①2Na2O2+2H2O=4NaOH+O2↑ ②2Na2O2+2CO2=2Na2CO3+O2 ③2Na2O2+4HCl=4NaCl+2H2O+O2↑ 由此可判断Na2O2( )
| A、是碱性氧化物 |
| B、可置于呼吸面具中提供O2 |
| C、无须密封保存 |
| D、投入水中会使溶液变红色 |
 某同学研究铝及其化合物的性质时设计了如下两个实验方案.
某同学研究铝及其化合物的性质时设计了如下两个实验方案.方案①:2.7g Al
| 100ml稀盐酸 |
| NaOH溶液 |
方案②:2.7g Al
| 100mlNaOH溶液 |
| 稀盐酸 |
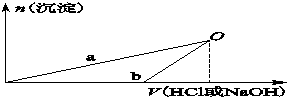
NaOH溶液和稀盐酸的浓度均是3mol/L,如图是向X溶液和Y溶液中分别加入NaOH溶液和稀盐酸时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法正确的是( )
| A、X溶液溶质为AlCl3,Y溶液溶质为NaAlO2 |
| B、b曲线表示的是向X溶液中加入NaOH溶液 |
| C、在O点时两方案中所得溶液浓度相等 |
| D、a、b曲线表示的反应都是氧化还原反应 |
常温下,下列物质的水溶液,其pH值大于7的是( )
| A、KNO3 |
| B、NaHSO4 |
| C、NH4Br |
| D、NaF |
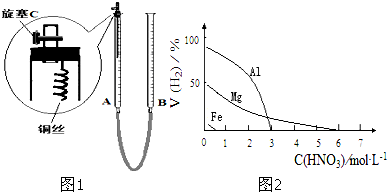
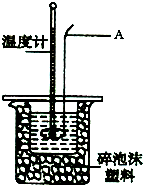 某实验小组用0.50mol?L-1NaOH溶液和0.50mol?L-1.1硫酸溶液进行中和热的测定.
某实验小组用0.50mol?L-1NaOH溶液和0.50mol?L-1.1硫酸溶液进行中和热的测定.
 某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.