题目内容
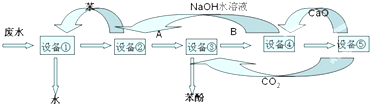
电子工业常用30%的FeCl3溶液腐蚀敷有铜箔的绝缘板,制成印刷线路板.为了从使用过的废腐蚀液中回收铜,并制得FeCl3溶液,拟采用下列实验.
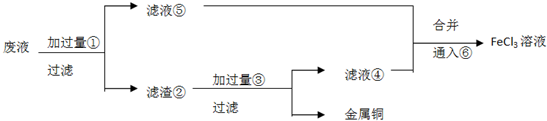
根据实验过程,思考,归纳并回答下列问题:
(1)检验Fe3+存在的试剂是
(2)写出FeCl3溶液与金属铜反应的离子方程式
(3)请写出上述实验中加入或生成的有关物质的化学式:
① 、② 、③ 、
④ 、⑤ 、⑥ .
(4)写出下列过程中反应的离子方程式:
ⅰ加入过量① 和
ⅱ加入过量③
ⅲ通入⑥ .

根据实验过程,思考,归纳并回答下列问题:
(1)检验Fe3+存在的试剂是
(2)写出FeCl3溶液与金属铜反应的离子方程式
(3)请写出上述实验中加入或生成的有关物质的化学式:
①
④
(4)写出下列过程中反应的离子方程式:
ⅰ加入过量①
ⅱ加入过量③
ⅲ通入⑥
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:由工艺流程可知,滤渣②中含有金属铜,目的是制取氯化铁,废液应该与过量的Fe反应,故①Fe;滤液⑤中含有FeCl2,通入⑥氯气可以得到氯化铁;滤渣②中含有金属Cu、未反应的Fe,加入③盐酸,过滤,回收铜,滤液④中含有FeCl2,与滤液⑤合并,制备氯化铁,
由上述分析可知:①Fe ②Fe和Cu ③HCl④FeCl2④⑤FeCl2⑥Cl2;
(1)检验溶液中Fe3+存在通常用KSCN溶液,溶液变红说明Fe3+存在;
(2)铜与氯化铁反应生成氯化铜、氯化亚铁;
(3)依据分析可知各物质为:Fe;Fe和Cu;HCl;FeCl2;FeCl2;Cl2;
(4)废液中氯化铁、氯化铜与过量的Fe反应;滤渣中含有金属铜、未反应的铁,加入盐酸,过滤,回收铜,滤液中含有氯化亚铁,与氯气反应制备氯化铁,据此进行书写离子方程式.
由上述分析可知:①Fe ②Fe和Cu ③HCl④FeCl2④⑤FeCl2⑥Cl2;
(1)检验溶液中Fe3+存在通常用KSCN溶液,溶液变红说明Fe3+存在;
(2)铜与氯化铁反应生成氯化铜、氯化亚铁;
(3)依据分析可知各物质为:Fe;Fe和Cu;HCl;FeCl2;FeCl2;Cl2;
(4)废液中氯化铁、氯化铜与过量的Fe反应;滤渣中含有金属铜、未反应的铁,加入盐酸,过滤,回收铜,滤液中含有氯化亚铁,与氯气反应制备氯化铁,据此进行书写离子方程式.
解答:
解:(1)检验溶液中Fe3+存在通常用KSCN溶液,取少量溶液与试管中,滴加KSCN溶液,溶液变红说明Fe3+存在,
故答案为:KSCN溶液;
(2)铜与氯化铁反应生成氯化铜、氯化亚铁,反应方程式为:2FeCl3+Cu═2 FeCl2+CuCl2,离子方程式为:2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
(3)由工艺流程可知,滤渣②中含有金属铜,目的是制取氯化铁,废液应该与过量的Fe反应,故①Fe;滤液⑤中含有FeCl2,通入⑥氯气可以得到氯化铁;滤渣②中含有金属Cu、未反应的Fe,加入③盐酸,过滤,回收铜,滤液④中含有FeCl2,与滤液⑤合并,制备氯化铁,向氯化亚铁溶液中通入氯气得到三氯化铁溶液,其反应的离子方程式为:2Fe2++C12=2Fe3++2C1-,由上述分析可知:①Fe ②Fe和Cu ③HCl④FeCl2④⑤FeCl2⑥Cl2;
故答案为:Fe;Fe和Cu;HCl;FeCl2;FeCl2;Cl2;
(4)过量的铁和废液中铁离子、铜离子反应,反应的离子方程式为:2Fe3++Fe=3Fe2+ 和 Fe+Cu2+=Fe2++Cu;
过量盐酸和滤渣中铁反应生成氯化亚铁和氢气,反应的离子方程式为:Fe+2H+=Fe2++H2↑;
氯气把亚铁离子氧化成铁离子,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;
故答案为:2Fe3++Fe=3Fe2+;Fe+Cu2+=Fe2++Cu;Fe+2H+=Fe2++H2↑;2Fe2++Cl2=2Fe3++2Cl-.
故答案为:KSCN溶液;
(2)铜与氯化铁反应生成氯化铜、氯化亚铁,反应方程式为:2FeCl3+Cu═2 FeCl2+CuCl2,离子方程式为:2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
(3)由工艺流程可知,滤渣②中含有金属铜,目的是制取氯化铁,废液应该与过量的Fe反应,故①Fe;滤液⑤中含有FeCl2,通入⑥氯气可以得到氯化铁;滤渣②中含有金属Cu、未反应的Fe,加入③盐酸,过滤,回收铜,滤液④中含有FeCl2,与滤液⑤合并,制备氯化铁,向氯化亚铁溶液中通入氯气得到三氯化铁溶液,其反应的离子方程式为:2Fe2++C12=2Fe3++2C1-,由上述分析可知:①Fe ②Fe和Cu ③HCl④FeCl2④⑤FeCl2⑥Cl2;
故答案为:Fe;Fe和Cu;HCl;FeCl2;FeCl2;Cl2;
(4)过量的铁和废液中铁离子、铜离子反应,反应的离子方程式为:2Fe3++Fe=3Fe2+ 和 Fe+Cu2+=Fe2++Cu;
过量盐酸和滤渣中铁反应生成氯化亚铁和氢气,反应的离子方程式为:Fe+2H+=Fe2++H2↑;
氯气把亚铁离子氧化成铁离子,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;
故答案为:2Fe3++Fe=3Fe2+;Fe+Cu2+=Fe2++Cu;Fe+2H+=Fe2++H2↑;2Fe2++Cl2=2Fe3++2Cl-.
点评:本题考查了化学工艺流程、常用化学用语和元素化合物性质等知识,Fe3+的检验为高频考点,题目难度不大,掌握元素化合物的性质是关键,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
下面是用盐酸滴定氢氧化钠的实验叙述:
①实验中的锥形瓶、滴定管都需润洗.
②滴定前锥形瓶中有水将使滴定结果偏小.
③加入2-3滴酚酞作指示剂.
④滴定时,左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶,眼睛注视锥形瓶中颜色的变化.
⑤滴定一旦发现溶液从红色变成无色,立即停止滴定.
⑥滴定终了时溶液的pH值刚好为7.
⑦若滴定前平视,滴定终点俯视,使结果偏小
上述相关说法中错误的是( )
①实验中的锥形瓶、滴定管都需润洗.
②滴定前锥形瓶中有水将使滴定结果偏小.
③加入2-3滴酚酞作指示剂.
④滴定时,左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶,眼睛注视锥形瓶中颜色的变化.
⑤滴定一旦发现溶液从红色变成无色,立即停止滴定.
⑥滴定终了时溶液的pH值刚好为7.
⑦若滴定前平视,滴定终点俯视,使结果偏小
上述相关说法中错误的是( )
| A、①②④⑤ | B、①②⑤⑦ |
| C、①②⑤⑥ | D、②⑤⑥⑦ |
某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+.将溶液滴在蓝色石蕊试纸上,试纸变红.取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀.下列判断合理的是( )
| A、一定有SO42-、Cl- |
| B、一定有SO42-、Al3+ |
| C、可能含有Al3+、Na+ |
| D、一定没有CO32-、Cl-、Na+ |
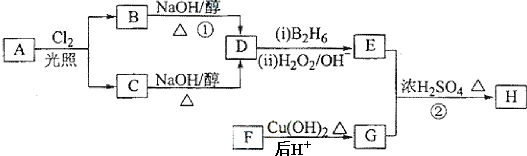
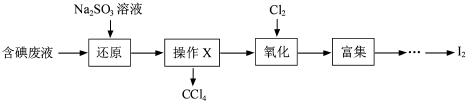
 G.
G.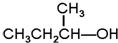 和
和