题目内容
常温时,溶液中下列各组离子一定能够大量共存的是( )
| A、Na+、OH-、AlO2-、S2- |
| B、K+、H+、Br-、HCO3- |
| C、Ba2+、Al3+、Cl-、SiO32- |
| D、K+、Fe3+、NO3-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.Na+、OH-、AlO2-、S2-离子之间不满足离子反应发生条件;
B.氢离子与碳酸氢根离子反应生成二氧化碳和水;
C.硅酸根离子与铝离子、钡离子发生反应;
D.K+、Fe3+、NO3-、SO42-离子之间不满足离子反应发生条件.
B.氢离子与碳酸氢根离子反应生成二氧化碳和水;
C.硅酸根离子与铝离子、钡离子发生反应;
D.K+、Fe3+、NO3-、SO42-离子之间不满足离子反应发生条件.
解答:
解:A.Na+、OH-、AlO2-、S2-之间不反应,在溶液中能够大量共存,故A正确;
B.H+、HCO3-之间发生反应生成二氧化碳气体,在溶液中不能大量共存,故B错误;
C.Ba2+、Al3+与SiO32-之间能够发生反应,在溶液中不能大量共存,故C错误;
D.K+、Fe3+、NO3-、SO42-之间不反应,在溶液中能够大量共存,故D正确;
故选AD.
B.H+、HCO3-之间发生反应生成二氧化碳气体,在溶液中不能大量共存,故B错误;
C.Ba2+、Al3+与SiO32-之间能够发生反应,在溶液中不能大量共存,故C错误;
D.K+、Fe3+、NO3-、SO42-之间不反应,在溶液中能够大量共存,故D正确;
故选AD.
点评:本题考查离子共存的正误判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能生成难溶物的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在55℃时,下列说法正确的是( )
| A、向水中加入少量硫酸氢钠固体,促进了水的电离,c(H+)增大,Kw不变 |
| B、pH=3的盐酸和pH=11的氨水等体积混合,溶液显碱性 |
| C、0.1mol/L的(NH4)2SO4溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D、pH=8的NaHCO3溶液中:c(OH-)=1×10-6mol/L |
在一定温度下,在恒定容积的密闭容器中进行的可逆反应A2(g)+B2(g)?2AB(g)达到化学平衡的标志是( )
| A、容器内的总压强不随时间而变化 | ||
B、反应速率V(A2)=V(B2)=
| ||
| C、单位时间内有n molA2生成的同时就有2n molAB生成 | ||
| D、容器内混合气体的密度不随时间而变化 |
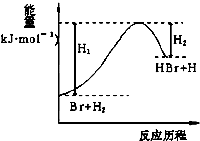 参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )| A、正反应为放热反应 |
| B、断键吸收的总能量大于成键放出的总能量 |
| C、反应物总能量高于生成物总能量 |
| D、升高温度可增大正反应速率,降低逆反应速率 |
下列各组离子在指定的溶液中一定能大量共存的是( )
| A、含有大量Fe3+的溶液:Na+、SCN-、Cl-、I- |
| B、氯水溶液:H+、Fe2+、Cl-、SO42- |
| C、常温下,pH=12的溶液:K+、Cl-、SO42-、SiO2- |
| D、与铝粉反应放出氢气的无色溶液中:Na+、NH4+、SO42-、AlO2- |
下列各组离子中,一定能够在指定溶液中大量共存的是( )
| A、能使酚酞变红的溶液中:Ba2+、Br-、AlO2-、ClO- |
| B、与铁反应能够产生H2的溶液中:Na+、Mg2+、NO3-、Cl- |
| C、PH=0 的溶液中:Fe3+、Al3+、HS-、SO42- |
| D、由水电离产生的C(H+)=1×10-12 mol/L的溶液:NH4+、Na+、NO3-、Cl- |
下列说法中正确的是( )
| A、同一原子中,1s、2s、3s电子的能量逐渐减小 |
| B、3p2表示3p能级有两个轨道 |
| C、处于最低能量状态的原子叫做基态原子 |
| D、同一原子中,2p、3p、4p能级的轨道数依次增多 |
有关化学用语正确的是( )
| A、乙烯的最简式C2H4 |
| B、乙醛的结构简式C2H4O |
C、四氯化碳的电子式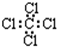 |
| D、乙酸乙酯的分子式C4H8O2 |
下列说法不正确的是( )
| A、石油分馏得到汽油、煤油和柴油是化学变化 |
| B、乙烯和苯是来自石油和煤的两种有机物,它们都能发生加成反应 |
| C、石油裂解得到乙烯、丙烯、丁二烯 |
| D、“西气东输”就是将新疆等地的天然气通过管道输到长江三角洲 |