题目内容
下列有关化学用语表示正确的是( )
| A、3-甲基-1-丁烯的结构简式:(CH3)2CHCH=CH2 |
B、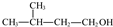 的名称是3-甲基丁醇 的名称是3-甲基丁醇 |
C、乙炔的分子结构模型示意图: |
D、CH4Si的结构式: |
考点:球棍模型与比例模型,结构式,结构简式
专题:
分析:A.根据烯烃的命名原则书写出该有机物的结构简式;
B.醇类的命名中,必须最长官能团羟基的位置;
C.乙炔分子为直线型结构,即所有的原子共直线;
D.碳和硅最外层都是4个电子,形成四条共价键,碳和硅之间应为双键.
B.醇类的命名中,必须最长官能团羟基的位置;
C.乙炔分子为直线型结构,即所有的原子共直线;
D.碳和硅最外层都是4个电子,形成四条共价键,碳和硅之间应为双键.
解答:
解:A.3-甲基-1-丁烯,该有机物主链为1-丁烯,在3号C含有1个甲基,其结构简式:(CH3)2CHCH=CH2,故A正确;
B.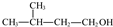 3-甲基丁醇,没有指出羟基的位置,正确命名应该为:3-甲基-1-丁醇,故B错误;
3-甲基丁醇,没有指出羟基的位置,正确命名应该为:3-甲基-1-丁醇,故B错误;
C.乙炔分子中所有原子都共直线,乙炔的结构模型为: ,故C错误;
,故C错误;
D.Si与C为同族元素,CH4Si的结构与乙烯类似,其结构式为: ,故D错误;
,故D错误;
故选A.
B.
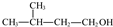 3-甲基丁醇,没有指出羟基的位置,正确命名应该为:3-甲基-1-丁醇,故B错误;
3-甲基丁醇,没有指出羟基的位置,正确命名应该为:3-甲基-1-丁醇,故B错误;C.乙炔分子中所有原子都共直线,乙炔的结构模型为:
 ,故C错误;
,故C错误;D.Si与C为同族元素,CH4Si的结构与乙烯类似,其结构式为:
 ,故D错误;
,故D错误;故选A.
点评:本题考查了结构式、比例模型、有机物命名、结构简式等知识,题目难度中等,注意掌握常见的化学用语的概念及正确表示方法,明确常见有机物空间结构.

练习册系列答案
相关题目
A、B、C、D、E五种元素具有相同的电子层数,A、B的最高价氧化物的水化物水溶液呈酸性,且酸性B>A;C、D的最高价氧化物的水化物的水溶液呈碱性,且碱性C>D;五种元素所形成的简单离子中,E的离子半径最小,则它们的原子序数由大到小的顺序是( )
| A、CDEAB |
| B、ECDAB |
| C、BAEDC |
| D、BADCE |
某元素的一价阴离子,核外有10个电子,则该元素的元素符号是( )
| A、K | B、F | C、Ne | D、Na |
 如图是17世纪炼金家们画的带有浓厚神秘色彩的两种同族元素的元素符号.已知X位于周期表前四周期,Y比X多1个电子层,X、Y都是生产半导体的材料,X的氢化物XH3有剧毒.下列推测不正确的是( )
如图是17世纪炼金家们画的带有浓厚神秘色彩的两种同族元素的元素符号.已知X位于周期表前四周期,Y比X多1个电子层,X、Y都是生产半导体的材料,X的氢化物XH3有剧毒.下列推测不正确的是( )| A、原子半径X>Y |
| B、最高价氧化物对应的水化物酸性X>Y |
| C、X的氢化物具有强还原性 |
| D、Y与碘同周期,Y最高价氧化物对应的水化物酸性比高碘酸(HIO4)强 |
下列各图所示的实验原理、方法、装置或操作正确的是( )
A、 称取固体质量 |
B、 收集NO气体 |
C、 配制溶液 |
D、 制取氨 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、标准状况下,28g氮气所含有的原子数目为NA |
| B、常温常压下,44.8L氯化氢气体所含的分子数为2NA |
| C、标准状况下,22.4L水中含有NA个水分子 |
| D、常温常压下,2.3 g Na+中含有的电子数为NA |
 (Ⅰ)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇.
(Ⅰ)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇.


