题目内容
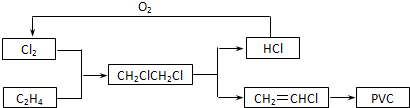
(2010?泰州三模)目前,聚氯乙烯塑料(PVC)占塑料消费量的30%以上,BICM法用乙烯、氯气等为原料合成PVC,其工艺流程如下.
(1)一定条件下,HCl与O2反应制取Cl2的方法称为地康法,其热化学反应方程式为:
4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-114.4kJ?mol-1.
升高温度,该反应的化学平衡常数K会
A.增大 B.减小 C.不变 D.无法确定
(2)一定温度下某体积可变的容器中充入4LHCl气体和6L空气(氧气占20%),充分反应后气体体积为9.2L.该反应中HCl气体的转化率为
(3)假设BICM法中各步反应的转化率均为100%,计算生产1000吨PVC需要购得的氯气质量.

(1)一定条件下,HCl与O2反应制取Cl2的方法称为地康法,其热化学反应方程式为:
4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-114.4kJ?mol-1.
升高温度,该反应的化学平衡常数K会
B
B
.A.增大 B.减小 C.不变 D.无法确定
(2)一定温度下某体积可变的容器中充入4LHCl气体和6L空气(氧气占20%),充分反应后气体体积为9.2L.该反应中HCl气体的转化率为
80%
80%
.(3)假设BICM法中各步反应的转化率均为100%,计算生产1000吨PVC需要购得的氯气质量.
分析:(1)该反应正反应是放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小;
(2)充分反应后气体体积变化为4L+6L-9.2L=0.8L,利用差量法计算计算参加反应的HCl的体积,再根据转化率定义计算;
(3)PVC是聚氯乙烯,其质量等于氯乙烯的质量,氯元素被完全利用生成氯乙烯,氯乙烯中氯元素的质量等于需要氯气的质量,根据氯乙烯中氯元素的质量分数计算需要氯气的质量.
(2)充分反应后气体体积变化为4L+6L-9.2L=0.8L,利用差量法计算计算参加反应的HCl的体积,再根据转化率定义计算;
(3)PVC是聚氯乙烯,其质量等于氯乙烯的质量,氯元素被完全利用生成氯乙烯,氯乙烯中氯元素的质量等于需要氯气的质量,根据氯乙烯中氯元素的质量分数计算需要氯气的质量.
解答:解:(1)该反应正反应是放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,
故答案为:B;
(2)充分反应后气体体积变化为4L+6L-9.2L=0.8L,
4HCl(g)+O2(g)?2Cl2(g)+2H2O(g) 体积减少△V
4 1
V(HCl) 0.8L
故V(HCl)=0.8L×4=3.2L,
故HCl气体的转化率为
×100%=80%,
故答案为:80%;
(3)PVC是聚氯乙烯,其质量等于氯乙烯的质量,氯元素被完全利用生成氯乙烯,氯乙烯中氯元素的质量等于需要氯气的质量,故需要氯气的质量为1000t×
=568t,
故答案为:568t.
故答案为:B;
(2)充分反应后气体体积变化为4L+6L-9.2L=0.8L,
4HCl(g)+O2(g)?2Cl2(g)+2H2O(g) 体积减少△V
4 1
V(HCl) 0.8L
故V(HCl)=0.8L×4=3.2L,
故HCl气体的转化率为
| 3.2L |
| 4L |
故答案为:80%;
(3)PVC是聚氯乙烯,其质量等于氯乙烯的质量,氯元素被完全利用生成氯乙烯,氯乙烯中氯元素的质量等于需要氯气的质量,故需要氯气的质量为1000t×
| 35.5 |
| 24+3+35.5 |
故答案为:568t.
点评:本题考查化学平衡常数的影响因素、化学计算等,(3)中计算为易错点、难点,注意氯元素完全利用,根据氯元素守恒计算,注意守恒思想的运用.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
 (2010?泰州三模)下列描述错误的是( )
(2010?泰州三模)下列描述错误的是( )