题目内容
12.用系统命名法命名下列物质或写出结构简式(1)
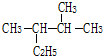 2,3-二甲基戊烷
2,3-二甲基戊烷(2)2-甲基-1-戊烯:CH2=C(CH3)CH2CH2CH3.
分析 判断有机物的命名是否正确或对有机物进行命名,其核心是准确理解命名规范:
(1)烷烃命名原则:
①长--选最长碳链为主链;
②多--遇等长碳链时,支链最多为主链;
③近--离支链最近一端编号;
④小--支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简--两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面.
(2)有机物的名称书写要规范;
(3)含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小.
解答 解:(1)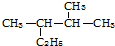 ,主链为烷烃,最长碳链含有5个C,主链为戊烷,编号从右边开始,在2、3号C各含有一个甲基,该有机物命名为:2,3-二甲基戊烷,
,主链为烷烃,最长碳链含有5个C,主链为戊烷,编号从右边开始,在2、3号C各含有一个甲基,该有机物命名为:2,3-二甲基戊烷,
故答案为:2,3-二甲基戊烷;
(2)依据系统命名方法,结合名称写出结构简式,2-甲基-1-戊烯的结构简式是:CH2=C(CH3)CH2CH2CH3,故答案为:CH2=C(CH3)CH2CH2CH3.
点评 本题考查了有机物的命名、有机物结构简式的书写,题目难度不大,注意掌握常见有机物的命名原则,能够根据命名写出有机物的结构简式.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
7.过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,探究了过氧化氢的性质,并准确测定了过氧化氢的含量.
Ⅰ.探究过氧化氢的性质
(1)该化学小组设计了两个实验,分别证明了H2O2的两个性质.请将他们的实验现象和验证性质填入下表:
(2)常温下,向H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+2H+下列说法正确的是ACD
A.H2O2的氧化性比Fe3+强,其还原性比Fe2+强
B.在H2O2分解过程中,溶液的pH逐渐下降
C.在H2O2分解过程中,Fe2+和Fe3+的总量发生变化
D.H2O2生产过程要严格避免混入Fe2+
Ⅱ.测定过氧化氢的含量
(1)量取10.00mL密度为ρ g/mL的过氧化氢溶液,溶解后将溶液转移至250mL容量瓶(填仪器名称)中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里.□MnO4-+□H2O2+□H+=□Mn2++□H2O+□□
该反应体现了H2O2的还原性.
(3)滴定时,将高锰酸钾标准溶液注入酸式 (填“酸式”或“碱式”)滴定管中.滴定到达终点的现象是滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色.
(4)反复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为$\frac{0.085cV}{ρ}$.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果偏高(填“偏高”或“偏低”或“不变”).
Ⅰ.探究过氧化氢的性质
(1)该化学小组设计了两个实验,分别证明了H2O2的两个性质.请将他们的实验现象和验证性质填入下表:
| 实验所用试剂或操作 | 实 验 现 象 | 验证的性质 |
| 碘化钾淀粉溶液 | ||
| 取适量过氧化氢溶液于试管中,加热,用带火星的木条检验. |
2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+2H+下列说法正确的是ACD
A.H2O2的氧化性比Fe3+强,其还原性比Fe2+强
B.在H2O2分解过程中,溶液的pH逐渐下降
C.在H2O2分解过程中,Fe2+和Fe3+的总量发生变化
D.H2O2生产过程要严格避免混入Fe2+
Ⅱ.测定过氧化氢的含量
(1)量取10.00mL密度为ρ g/mL的过氧化氢溶液,溶解后将溶液转移至250mL容量瓶(填仪器名称)中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里.□MnO4-+□H2O2+□H+=□Mn2++□H2O+□□
该反应体现了H2O2的还原性.
(3)滴定时,将高锰酸钾标准溶液注入酸式 (填“酸式”或“碱式”)滴定管中.滴定到达终点的现象是滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色.
(4)反复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为$\frac{0.085cV}{ρ}$.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果偏高(填“偏高”或“偏低”或“不变”).
17.下列叙述中正确的是( )
| A. | 含5个碳原子的有机物,每个分子中最多可形成4个C-C键 | |
| B. | 正戊烷分子中所有原子均在一条直线上 | |
| C. | 碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定符合通式CnH2n+2 | |
| D. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 |
4.有关乙醇(C2H5OH)的说法正确的是( )
| A. | 乙醇是食醋的主要成分 | |
| B. | C2H5OH中C、H、O元素的质量比是2:6:1 | |
| C. | 乙醇不能溶于水 | |
| D. | C2H5OH中C元素的质量分数是$\frac{12×2}{12×2+1×6+16×1}$ |
1.2011年3月18日至19日,受“吃碘盐能防止核辐射”等谣言的影响,我国部分地区出现抢购食盐现象.已知碘盐的主要成分是KIO3和NaCl,KIO3与NaHSO3发生反应:2KIO3+6NaHSO3═2KI+3Na2SO4+3H2SO4,下列说法中不正确的是( )
| A. | 23Na37Cl中质子数和中子数之比是7:8 | |
| B. | KIO3和NaHSO3都是强电解质 | |
| C. | KIO3作氧化剂发生氧化反应 | |
| D. | 生成1mo1KI时,转移6mo1电子 |
2.在下列物质的溶液中,滴加氢氧化钠溶液,能产生蓝色沉淀的是( )
| A. | CuSO4 | B. | FeCl3 | C. | HCl | D. | H2SO4 |
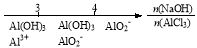
 氨水与SO2反应后溶液中的铵盐:
氨水与SO2反应后溶液中的铵盐: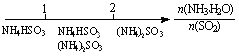
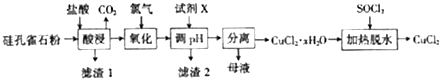
 .
.