题目内容
5.写出铜与稀硝酸反应的化学方程式3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,该反应中硝酸的作用是氧化剂和酸的作用.分析 Cu与稀硝酸反应生成硝酸铜、NO和水,据此书写方程式;根据化合价的变化确定硝酸的性质,由此分析解答.
解答 解:Cu与稀硝酸反应生成硝酸铜、NO和水,反应的化学方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,反应中硝酸的化合价部分降低,部分未变,所以硝酸是氧化剂和酸的作用,
故答案为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O; 氧化剂和酸的作用.
点评 本题考查了硝酸性质,硝酸强氧化性能与不活泼的金属铜反应生成氮的氧化物、根据化合价的变化,来确定硝酸的化学性质是解题关键,题目难度中等.

练习册系列答案
相关题目
15.常温下,部分弱酸的电离平衡常数如表:
下列选项错误的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K1=1.8×10-5 | K1=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 等物质的量浓度时:pH(Na2CO3)>pH(NaCN)>pH(NaHCO3)>pH(CH3COONa) | |
| B. | 中和等体积、等pH的CH3COOH溶液和HCN溶液消耗NaOH的量前者大于后者 | |
| C. | 向NaCN中通入少量的CO2:CN -+H2O+CO2=HCO3 -+HCN | |
| D. | 0.2mol/L HCN与0.1mol/L NaOH溶液等体积混合后显碱性,则c(Na+)>c(CN-) |
16.化学反应速率是通过实验测定的,下列化学反应速率的测量中,测量依据不可行的是( )
| 选项 | 化学反应 | 测量依据(单位时间内) |
| A | CO(g)+H2O(g)=CO2(g)+H2(g) | 压强变化 |
| B | Zn+H2SO4=ZnSO4+H2 | H2体积 |
| C | 2NO2?N2O4 | 颜色深浅 |
| D | Ca(OH)2+Na2CO3=CaCO3↓+2NaOH | 沉淀质量 |
| A. | A | B. | B | C. | C | D. | D |
20.下列叙述正确的是( )
| A. | 1 mol H3PO4的质量为98g.mol-1 | B. | H3PO4的摩尔质量为98 g | ||
| C. | 9.8 g H3PO4含有NA个H3PO4分子? | D. | NA个H3PO4分子的质量为98g |
10.下列气体在同温同压时,密度最大的是( )
| A. | O2 | B. | SO2 | C. | Cl2 | D. | NH3 |
17.X 元素最高价氧化物的水化物化学式为 H2XO4,则 X的气态氢化物的化学式为( )
| A. | XH4 | B. | XH3 | C. | H2X | D. | HX |
14.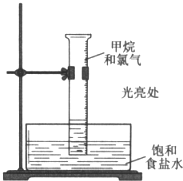 甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )
甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )
 甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )
甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )| 现象 | 解释 | |
| A. | 量筒内气体颜色逐渐变浅 | 甲烷被氯气还原 |
| B. | 量筒内出现少量白雾 | 生成HCl气体 |
| C. | 量筒内壁产生油状液滴 | 油状液体是CCl4 |
| D. | 量筒中液面降低 | 生成液态产物 |
| A. | A | B. | B | C. | C | D. | D |
15.下列电离方程式正确的是( )
| A. | NaHCO3═Na++H++CO32- | B. | H2SO4═2H++SO42- | ||
| C. | FeCl3═Fe3++Cl3- | D. | Ba(OH)2═Ba2++2OH- |