题目内容
3.已知33As、35Br位于同一周期.某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X.(1)已知KBrO3在反应中得到电子,则该反应的还原剂是AsH3.已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式是Br2.
(2)在该反应条件下可推知ac(填序号).
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X d.还原性:X>AsH3
(3)该反应的氧化剂和还原剂的物质的量之比为8:5; KBrO3与HBr反应也会生成X,则该反应中氧化剂和还原剂的物质的量之比为1:5.
分析 由信息可知,该反应中氧化剂是KBrO3,还原剂是AsH3,溴元素化合价变化为由+5价降低,As元素化合价变化为-3→+5价,
(1)化合价升高元素所在的反应物是还原剂;根据溴元素化合价的降低情况来计算;
(2)根据氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性,据此判断;
(3)根据氧化剂化合价降低得电子,还原剂化合价升高失电子结合得失电子守恒进行计算.
解答 解:(1)KBrO3在反应中得到电子,所以KBrO3化合价降低是氧化剂,AsH3变成了H3AsO4,所以AsH3是还原剂,设X中溴元素的化合价为x,则0.2mol(5-x)=1mol,所以x=0,故X为Br2,故答案为:AsH3;Br2;
(2)a、反应中KBrO3是氧化剂,H3AsO4是氧化产物,氧化性为KBrO3>H3AsO4,故a正确,b错误;
c、AsH3是还原剂,X是还原产物,所以还原性AsH3>X,故c正确,故d错误.
故选:ac;
(3)还原剂AsH3中化合价升高的元素是砷元素,化合价从-3价升到+5价升高8,氧化剂KBrO3中化合价降低的元素是溴元素,化合价从+5价降到0价降低5,根据得失电子守恒,所以氧化剂和还原剂的物质的量之比为8:5;KBrO3与HBr反应也会生成X,则还原剂HBr中化合价升高的元素是Br元素,化合价从-1价升到0价升高1,氧化剂KBrO3中化合价降低的元素是溴元素,化合价从+5价降到0价降低5,根据得失电子守恒,所以氧化剂和还原剂的物质的量之比为1:5,
故答案为:8:5;1:5.
点评 本题考查氧化还原反应,为高考常见题型,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念和转移电子的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
4.下列说法不正确的是( )
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 伴有能量变化的物质变化不一定都是化学反应 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同 | |
| D. | 在一个确定的化学反应关系中,反应物的总能量总是大于生成物的总能量 |
14.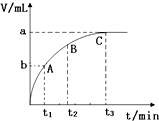 为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
(1)过氧化氢分解的化学方程式为2H2O2$\frac{\underline{\;三氯化铁\;}}{\;}$2H2O+O2↑.
(2)实验①的目的是探究温度对H2O2分解速率的影响,实验中滴加FeCl3溶液的目的是加快H2O2分解速率,使实验现象易于观察.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/LFeCl3溶液,观察产生气泡的速率(用实验中所提供的几种试剂).
(4)某同学在50mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是C,最快的是A.
 为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.| 编号 | 操 作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中. | 试管A中不再产生气泡,试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液. | 试管A、B中均未见气泡产生 |
(2)实验①的目的是探究温度对H2O2分解速率的影响,实验中滴加FeCl3溶液的目的是加快H2O2分解速率,使实验现象易于观察.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/LFeCl3溶液,观察产生气泡的速率(用实验中所提供的几种试剂).
(4)某同学在50mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是C,最快的是A.
11.只含非金属元素的晶体描述正确的是( )
| A. | 有可能是金属晶体 | B. | 有可能是离子晶体 | ||
| C. | 一定是分子晶体 | D. | 一定不是原子晶体 |
18.表是一些共价键的键能(kJ/mol)数据,以下表达中肯定正确的是( )
| 共价键 | 键能 | 共价键 | 键能 |
| H-H | 436 | H-F | 565 |
| C-F | 427 | H-S | 339 |
| C-Cl | 330 | H-Se | 314 |
| A. | H2(g)→2H (g)-436kJ | |
| B. | 键长越短,共价键越牢固 | |
| C. | 相同条件下CH3F比CH3Cl更 易发生水解反应 | |
| D. | 相同压强下,H2S的沸点比 H2Se的沸点高 |
8.科学家将液态的金属镓(Ga)充入碳纳米管中,发明出一种世界上最小的温度计-碳纳米管温度计.该温度计通过电子显微镜进行读数,精确度较高,其测量范围在18℃~490℃.下列说法错误的是( )
| A. | 碳纳米管中的镓为液体 | |
| B. | 金属镓的体积在10℃~500℃之间随温度的变化比较均匀 | |
| C. | 碳纳米管的体积在10℃~500℃之间随温度的变化很小 | |
| D. | Al(OH)3、Ga(OH)3均是两性氧化物 |
15.设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,2.24 L Cl4中含CL原子数目为0.4NA | |
| B. | 白磷分子(P4)呈正四面体结构,12.4g白磷中含有P-P键数目为0.6NA | |
| C. | 5.6g铁粉在2.24 L(标准状况)氯气中充分燃烧,失去的电子书为0.3NA | |
| D. | 常温常压下10g46%酒精溶液中含氧原子总数为 0.3NA |
12.下列关于化学式为[TiCl(H2O)5]Cl2•H2O的配合物的说法中正确的是( )
| A. | 配体是Cl-和H2O,配位数是9 | |
| B. | 中心离子是Ti3+,配离子是[TiCl(H2O)5]2+ | |
| C. | 内界和外界中的Cl-的数目比是 2:1 | |
| D. | 加入足量AgNO3溶液,所有Cl-均被完全沉淀 |
13.向amolKOH的溶液中通入bmolSO2,下列说法不正确的是( )
| A. | 当a>2b时,发生的离子反应为:2OH-+SO2=SO32-+H2O | |
| B. | 当a<b时,发生的离子反应为:OH-+SO2=HSO3- | |
| C. | 当2a=3b时,发生的离子反应为:3OH-+2SO2=SO32-+HSO3-+H2O | |
| D. | 当0.5a<b<a时,溶液中HSO3-与SO32-的物质的量之比为(a-b):(2b-a) |