��Ŀ����
Һ����������������ش���������
��1��һ�����������ܱ������з�����Ӧ��
a��NH4I(s)  NH3(g) + HI(g)
NH3(g) + HI(g)
b��2HI(g)  H2(g) + I2(g)
H2(g) + I2(g)
��д����Ӧa��ƽ�ⳣ������ʽ
�ڴﵽƽ������������������Ӧb���ƶ����� ��������������ƶ��������ﵽ�µ�ƽ��ʱ��������ɫ�������仯 ������������dz�����䡱��
��2����ҵ�Ϻϳɰ��ķ�Ӧ��N2(g)��3H2(g)  2NH3(g) ��H����92.60 kJ��mol��1
2NH3(g) ��H����92.60 kJ��mol��1
����˵����˵��������Ӧ������Ӧ������е���________(�����)��
a.��λʱ��������2n mol NH3��ͬʱ����3n mol H2
b.��λʱ��������6n mol N��H����ͬʱ����2n mol H��H��
c.��N2��H2��NH3�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����֮��Ϊ1��3��2
d.��������ƽ��Ħ����������
e.�����ڵ������ܶȲ���
��3����֪�ϳɰ���Ӧ��ij�¶���2 L���ܱ������н��У�����������ݣ�

���ݱ������ݼ��㣺
�ٷ�Ӧ���е�2 hʱ�ų�������Ϊ________ kJ��
��0��1 h��N2��ƽ����Ӧ����Ϊ________ mol��L��1��h��1��
�۴��¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K��________(������λС��)��
�ܷ�Ӧ�ﵽƽ�������ƽ����ϵ���ټ���N2��H2��NH3��1.00 mol����ѧƽ�⽫��________�����ƶ�(�����Ӧ�����淴Ӧ��)��
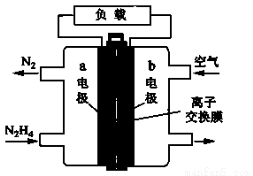
��4���£�N2H4��������������NH3����������ˮ����ˮ��Ӧ����һ�ֶ�Ԫ��������Һ�зֲ����룬�������ӷ�Ӧ����ʽ��ʾ��ˮ��Һ�Լ��Ե�ԭ�� ��
����18�֣���1���� k��c(NH3)?c(HI) (2�� ) �� ���ƶ� (2�� ) ��dz(2�� )
��2�� b��d (2�� )
��3����27.78 (2�� ) ��0.05 (2�� ) ��0.15 (2�� ) ������Ӧ(2�� )
��4��N2H4��2H2O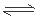 [N2H5��H2O]+ + OH�� (2�� )
[N2H5��H2O]+ + OH�� (2�� )
��������
�����������1���� ��ӦNH4I(s) 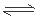 NH3(g) + HI(g) ƽ�ⳣ������ʽ��k��c(NH3)?c(HI) �� ��Ӧ2HI(g)
NH3(g) + HI(g) ƽ�ⳣ������ʽ��k��c(NH3)?c(HI) �� ��Ӧ2HI(g) 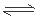 H2(g) + I2(g)�����Ƿ�Ӧǰ�����������ȵķ�Ӧ���ﵽƽ����������������2HI(g)
H2(g) + I2(g)�����Ƿ�Ӧǰ�����������ȵķ�Ӧ���ﵽƽ����������������2HI(g) 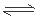 H2(g) + I2(g)���ƶ��������������ݻ��������Դﵽ�µ�ƽ��ʱ��������ɫ��dz����2��a.��λʱ��������2n mol NH3��ͬʱ����3n mol H2����Ӧ����ƽ��״̬������ b.��λʱ��������6n mol N��H����ͬʱ����2n mol H��H������Ӧ������У���ȷ��c.��N2��H2��NH3�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����֮��Ϊ1��3��2���κ�״̬�¶����ڵ�״̬������ȷ����Ӧ���еķ����̶ȣ�����d.���ڵ�һ����Ӧ�������������ķ�Ӧ�������ӳδ�ﵽƽ��״̬����Ӧ������У�������������������ɸ��ߵĹ����Ϊ���壬�����������ʵ������䣬���Ի�������ƽ��Ħ������������ȷ��e.���۷�Ӧ�Ƿ���ƽ��״̬�������ڵ������ܶȲ��䣬��˲���ȷ����Ӧ���еķ�����3���ٸ��ݷ���ʽ��֪1mol�ĵ�����ȫ��Ӧ�ų�������92.60 kJ����Ӧ���е�2 hʱN2������Ӧ������0.3mol����ų�������Ϊ92.60 kJ/mol��0.3mol=27.78KJ����0��1 h��H2��ƽ����Ӧ����ΪV(H2)=(4.50-4.20)mol��2 L��1h=0.15(mol/L?h)������V(H2)=3V(N2)������V(N2)= V(H2) ��3=0.05(mol/L?h)���۵���Ӧ�ﵽƽ��ʱ��c(N2)=0. 5mol/L c(H2)=1. 5mol/L, c(NH3)=0. 5mol/L,���¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K��
H2(g) + I2(g)���ƶ��������������ݻ��������Դﵽ�µ�ƽ��ʱ��������ɫ��dz����2��a.��λʱ��������2n mol NH3��ͬʱ����3n mol H2����Ӧ����ƽ��״̬������ b.��λʱ��������6n mol N��H����ͬʱ����2n mol H��H������Ӧ������У���ȷ��c.��N2��H2��NH3�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����֮��Ϊ1��3��2���κ�״̬�¶����ڵ�״̬������ȷ����Ӧ���еķ����̶ȣ�����d.���ڵ�һ����Ӧ�������������ķ�Ӧ�������ӳδ�ﵽƽ��״̬����Ӧ������У�������������������ɸ��ߵĹ����Ϊ���壬�����������ʵ������䣬���Ի�������ƽ��Ħ������������ȷ��e.���۷�Ӧ�Ƿ���ƽ��״̬�������ڵ������ܶȲ��䣬��˲���ȷ����Ӧ���еķ�����3���ٸ��ݷ���ʽ��֪1mol�ĵ�����ȫ��Ӧ�ų�������92.60 kJ����Ӧ���е�2 hʱN2������Ӧ������0.3mol����ų�������Ϊ92.60 kJ/mol��0.3mol=27.78KJ����0��1 h��H2��ƽ����Ӧ����ΪV(H2)=(4.50-4.20)mol��2 L��1h=0.15(mol/L?h)������V(H2)=3V(N2)������V(N2)= V(H2) ��3=0.05(mol/L?h)���۵���Ӧ�ﵽƽ��ʱ��c(N2)=0. 5mol/L c(H2)=1. 5mol/L, c(NH3)=0. 5mol/L,���¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K��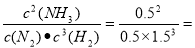 0.15; �ܷ�Ӧ�ﵽƽ�������ƽ����ϵ���ټ���N2��H2��NH3��1.00 mol�������ڷ�Ӧ���Ũ������Ķ࣬���Ի�ѧƽ�⽫������Ӧ�����ƶ�����4���£�N2H4��������������NH3����������ˮ����ˮ��Ӧ����һ�ֶ�Ԫ��������Һ�зֲ����룬ˮ��Һ�Լ��������ڴ��ڵ���ƽ�⣺N2H4��2H2O
0.15; �ܷ�Ӧ�ﵽƽ�������ƽ����ϵ���ټ���N2��H2��NH3��1.00 mol�������ڷ�Ӧ���Ũ������Ķ࣬���Ի�ѧƽ�⽫������Ӧ�����ƶ�����4���£�N2H4��������������NH3����������ˮ����ˮ��Ӧ����һ�ֶ�Ԫ��������Һ�зֲ����룬ˮ��Һ�Լ��������ڴ��ڵ���ƽ�⣺N2H4��2H2O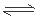 [N2H5��H2O]+ + OH����
[N2H5��H2O]+ + OH����
���㣺���黯ѧ��Ӧ���ʡ���ѧƽ���ƶ�����Ӧ�Ļ�ѧƽ�ⳣ���ļ��㡢�ƶ��������ʵ���Һ������Ե�ԭ�������֪ʶ��

 2SO3(g)��ƽ����ϵ�м���18O2���ﵽ�µ�ƽ���18Oֻ������O2��SO3��
2SO3(g)��ƽ����ϵ�м���18O2���ﵽ�µ�ƽ���18Oֻ������O2��SO3��