题目内容
下列叙述正确的是( )
| A、Cl-Cl、Br-Br、I-I的键长逐渐增大,键能也逐渐增大 | B、碘的晶体中碘分子之间的范德华力小于氯的晶体中氯分子之间的范德华力 | C、H2SO4、H3PO4、HClO4的酸性依次减弱 | D、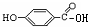 的沸点比 的沸点比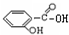 的沸点高 的沸点高 |
分析:A、键长越长,键能越小;
B、组成和结构相似的分子晶体,相对分子质量越大,范德华力越大;
C、同周期元素的原子,从左到右,得电子能力增强,它们的最高价氧化物的水化物酸性逐渐增强;
D、分子间氢键使得物质的熔、沸点升高,分子内氢键使得物质的熔、沸点降低;
B、组成和结构相似的分子晶体,相对分子质量越大,范德华力越大;
C、同周期元素的原子,从左到右,得电子能力增强,它们的最高价氧化物的水化物酸性逐渐增强;
D、分子间氢键使得物质的熔、沸点升高,分子内氢键使得物质的熔、沸点降低;
解答:解:A、Cl-Cl、Br-Br、I-I的键长逐渐增大,键能逐渐越小,故A错误;
B、组成和结构相似的分子晶体,相对分子质量越大,范德华力越大,所以碘的晶体中碘分子之间的范德华力大于氯的晶体中氯分子之间的范德华力,故B错误;
C、同周期元素的原子,从左到右,得电子能力增强,它们的最高价氧化物的水化物酸性逐渐增强,所以酸性:HClO4>H2SO4>H3PO4,故C错误;
D、 形成分子间氢键,使得物质的沸点升高;
形成分子间氢键,使得物质的沸点升高; 形成分子内氢键,使得物质的沸点降低,所以
形成分子内氢键,使得物质的沸点降低,所以 的沸点比
的沸点比 的沸点高,故D正确;
的沸点高,故D正确;
故选:D;
B、组成和结构相似的分子晶体,相对分子质量越大,范德华力越大,所以碘的晶体中碘分子之间的范德华力大于氯的晶体中氯分子之间的范德华力,故B错误;
C、同周期元素的原子,从左到右,得电子能力增强,它们的最高价氧化物的水化物酸性逐渐增强,所以酸性:HClO4>H2SO4>H3PO4,故C错误;
D、
 形成分子间氢键,使得物质的沸点升高;
形成分子间氢键,使得物质的沸点升高; 形成分子内氢键,使得物质的沸点降低,所以
形成分子内氢键,使得物质的沸点降低,所以 的沸点比
的沸点比 的沸点高,故D正确;
的沸点高,故D正确;故选:D;
点评:本题主要考查了物质的性质与结构的关系规律,难度不大,注意规律的掌握.

练习册系列答案
相关题目