题目内容
17.按要求完成下列填空.(1)同温同压下烷烃A蒸气的密度是H2的15倍,烷烃A的分子式:C2H6;结构简式CH3CH3.
(2)烷烃B的分子中含有200个氢原子,烷烃B的分子式:C99H200.
(3)含有5个碳原子的烷烃D,烷烃D的分子式:C5H12.
(4)分子中含有22个共价键的烷烃,烷烃的分子式:C7H16.
分析 (1)根据密度之比等于相对分子质量之比计算A的相对分子质量,结合烷烃的组成通式确定分子式,书写可能的结构简式;
(2)根据烷烃的组成通式CnH2n+2确定分子式;
(3)根据烷烃的组成通式CnH2n+2确定分子式;
(4)烷烃CnH2n+2中含有(n-1)个碳碳单键、(2n+2)个C-H单键.
解答 解:(1)根密度之比等于相对分子质量之比,A的相对分子质量为15×2=30,烷烃的组成通式CnH2n+2,则14n+2=30,解得n=2,故该烷烃的分子式为C2H6,结构简式为:CH3CH3,
故答案为:C2H6;CH3CH3;
(2)烷烃的组成通式CnH2n+2,故2n+2=200,解得n=99,故该烷烃的分子式为:C99H200,
故答案为:C99H200;
(3)烷烃D含有5个碳原子,则H原子数目为5×2+2=12,故D的分子式为:C5H12,
故答案为:C5H12;
(4)烷烃CnH2n+2中含有(n-1)个碳碳单键、(2n+2)个C-H单键,则(n-1)+(2n+2)=22,解得n=7,故该烷烃的分子式为:C7H16,
故答案为:C7H16.
点评 本题考查烷烃分子式确定,题目贴近基础,比较基础,注意利用烷烃的组成通式进行解答,理解烷烃的结构特点.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
7.下列括号内有关物质的描述及用途错误的是( )
| A. | 硅(半导体材料) | B. | 二氧化硅(制光导纤维) | ||
| C. | Na2Si03 (用作粘合剂,俗称水玻璃) | D. | Al(OH)3(用作胃药,俗称人造刚玉) |
8.根据元素周期律进行推断,下列不正确的是( )
| A. | 碱性:KOH>NaOH | B. | Mg、Al与同浓度盐酸反应,Mg更剧烈 | ||
| C. | 稳定性:HBr>HI | D. | 酸性:H3PO4>HNO3 |
5.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A. | 粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu-2e-═Cu2+ | |
| B. | 氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- | |
| C. | 用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-═Cl2↑ | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
12.某固体化合物A不导电,但熔化或溶于水都能完全电离.下列关于物质A的说法中,正确的是( )
| A. | A是非电解质 | B. | A是强电解质 | C. | A是共价化合物 | D. | A是弱电解质 |
2.Ni2O3是灰黑色无气味、有光泽的固体,主要用作陶瓷、玻璃、搪瓷的着色颜料,也经常用于制造镍电池.某实验室尝试用工业废弃的NiO催化剂(还含有Fe2O3、CaO、CuO、BaO等杂质)为原料制备Ni2O3,实验工艺流程为如图1:
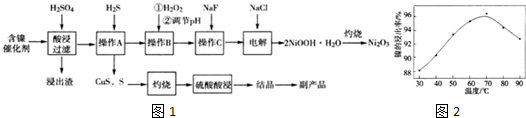
已知:①有关氢氧化物开始沉淀和沉淀完全的pH如表:
②常温时CaF2的溶度积常数为2.7×10-11.
(1)流程中酸浸后浸出渣包含多种成分.最难溶的强电解质的化学式为BaSO4.
(2)实验人员发现温度不同时,镍的浸出率不同,浸出率与温度的关系如图2所示.请解释当温度高于70℃时,浸出液中Ni2+含量降低的原因:温度升高,Ni2+的水解程度增大,浸出渣中Ni(OH)2含量增大,浸出率降低.
(3)操作A的名称为过滤,操作B中需调节溶液的pH,所需调节的pH范围为3.7-7.7,操作C的目的是除去溶液中的Ca2+.
(4)电解步骤中,Cl-首先在阳极被氧化为ClO-,然后C1O-将Ni2+氧化成2NiOOH•H2O沉淀.写出生成沉淀反应的离子方程式:ClO-+2Ni2++4OH-=2NiOOH.H2O+Cl-.若实验最后得到Ni2O3 33,.2g,则电解过程中,电路中转移的电子数至少为2.41×1023 个.

已知:①有关氢氧化物开始沉淀和沉淀完全的pH如表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH02 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
(1)流程中酸浸后浸出渣包含多种成分.最难溶的强电解质的化学式为BaSO4.
(2)实验人员发现温度不同时,镍的浸出率不同,浸出率与温度的关系如图2所示.请解释当温度高于70℃时,浸出液中Ni2+含量降低的原因:温度升高,Ni2+的水解程度增大,浸出渣中Ni(OH)2含量增大,浸出率降低.
(3)操作A的名称为过滤,操作B中需调节溶液的pH,所需调节的pH范围为3.7-7.7,操作C的目的是除去溶液中的Ca2+.
(4)电解步骤中,Cl-首先在阳极被氧化为ClO-,然后C1O-将Ni2+氧化成2NiOOH•H2O沉淀.写出生成沉淀反应的离子方程式:ClO-+2Ni2++4OH-=2NiOOH.H2O+Cl-.若实验最后得到Ni2O3 33,.2g,则电解过程中,电路中转移的电子数至少为2.41×1023 个.
7.合成氨是工业上的重要反应:N2(g)+3H2(g)$?_{催化剂}^{高温高压}$2NH3(g),下列说法不正确的是( )
| A. | 反应达到平衡状态后,各物质浓度不变,反应停止 | |
| B. | 反应达到平衡状态后,单位时间内生成1molN2的同时消耗3molH2 | |
| C. | 在上述条件下,N2不可能100%转化为NH3 | |
| D. | 使用催化剂是为了加快反应速率,提高生产效率 |
 ,它是由σ键形成的(根据原子轨道的重叠程度填写).
,它是由σ键形成的(根据原子轨道的重叠程度填写).