题目内容
已知:将Cl2通入适量KOH溶液,产物中可能有KC1、KClO、KC1O3,且
的值与温度高低有关.当n(KOH)=amol时,下列有关说法错误的是( )
| c(Cl-) |
| c(ClO-) |
A、若某温度下,反应后C(Cl-):C(ClO-)=11,则溶液中C(ClO-):C(ClO3-)=
| ||||
B、参加反应的氯气的物质的量等于
| ||||
C、改变温度,反应中转移电子的物质的量n的范围:
| ||||
D、改变温度,产物中KC1O3的最大理论产量为
|
考点:氯气的化学性质,化学方程式的有关计算
专题:卤族元素
分析:A.令n(ClO-)=1mol,反应后C(Cl-):C(ClO-)=11,则n(Cl-)=11mol,根据电子转移守恒计算n(ClO3-),据此计算判断;
B.由Cl原子守恒可知,2n(Cl2)=n(KCl)+n(KClO)+n(KClO3),由钾离子守恒可知n(KCl)+n(KClO)+n(KClO3)=n(KOH);
C.氧化产物只有KClO3时,转移电子最多,氧化产物只有KClO时,转移电子最少,根据电子转移守恒及钾离子守恒计算;
D.氧化产物只有KClO3时,其物质的量最大,结合C中计算判断.
B.由Cl原子守恒可知,2n(Cl2)=n(KCl)+n(KClO)+n(KClO3),由钾离子守恒可知n(KCl)+n(KClO)+n(KClO3)=n(KOH);
C.氧化产物只有KClO3时,转移电子最多,氧化产物只有KClO时,转移电子最少,根据电子转移守恒及钾离子守恒计算;
D.氧化产物只有KClO3时,其物质的量最大,结合C中计算判断.
解答:
解:A.令n(ClO-)=1mol,反应后C(Cl-):C(ClO-)=11,则n(Cl-)=11mol,电子转移守恒,5×n(ClO3-)+1×n(ClO-)=1×n(Cl-),即5×n(ClO3-)+1×1mol=1×11mol,解得n(ClO3-)=2mol,故溶液中C(ClO-):C(ClO3-)=
,故A正确;
B.由Cl原子守恒可知,2n(Cl2)=n(KCl)+n(KClO)+n(KClO3),由钾离子守恒可知n(KCl)+n(KClO)+n(KClO3)=n(KOH),故参加反应的氯气的物质的量=
n(KOH)=
amol,故B正确;
C.氧化产物只有KClO3时,转移电子最多,根据电子转移守恒n(KCl)=5(KClO3),由钾离子守恒:n(KCl)+n(KClO3)=n(KOH),故n(KClO3)=
n(KOH)=
a mol,转移电子最大物质的量=
a mol×5=
a mol,氧化产物只有KClO时,转移电子最少,根据电子转移守恒n(KCl)=n(KClO),由钾离子守恒:n(KCl)+n(KClO)=n(KOH),故n(KClO)=
n(KOH)=
amol,转移电子最小物质的量=
amol×1=
amol,故反应中转移电子的物质的量ne的范围:
amol≤n≤
amol,故C正确;
D.氧化产物只有KClO3时,其物质的量最大,由C中计算可知:n最大(KClO3)=
n(KOH)=
a mol,故D错误,
故选D.
| 1 |
| 2 |
B.由Cl原子守恒可知,2n(Cl2)=n(KCl)+n(KClO)+n(KClO3),由钾离子守恒可知n(KCl)+n(KClO)+n(KClO3)=n(KOH),故参加反应的氯气的物质的量=
| 1 |
| 2 |
| 1 |
| 2 |
C.氧化产物只有KClO3时,转移电子最多,根据电子转移守恒n(KCl)=5(KClO3),由钾离子守恒:n(KCl)+n(KClO3)=n(KOH),故n(KClO3)=
| 1 |
| 6 |
| 1 |
| 6 |
| 1 |
| 6 |
| 5 |
| 6 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 5 |
| 6 |
D.氧化产物只有KClO3时,其物质的量最大,由C中计算可知:n最大(KClO3)=
| 1 |
| 6 |
| 1 |
| 6 |
故选D.
点评:本题考查氧化还原反应计算,难度中等,注意电子转移守恒及极限法的应用.

练习册系列答案
相关题目
某一定量的气态烷烃在氧气中完全燃烧生成a mol二氧化碳和b mol水,则下列说法正确的是( )
| A、该烷烃的物质的量为(b-a)mol |
| B、该烷烃的物质的量为a mol |
| C、该烷烃的物质的量为(b-a)/2 mol |
| D、不能求出该烷烃的物质的量 |
下列各组离子在水溶液中能够大量共存的是( )
| A、K+、Cl-、SO42- |
| B、SO42-、Ca2+、CO32- |
| C、H+、CO32-、Cl- |
| D、Fe3+、OH-、NO3- |
下列解释事实的化学方程式或离子方程式正确的是( )
| A、用食醋除去暖水瓶中的水垢:2CH3COOH+CaCO3═Ca2++2CH3COO-+CO2↑+H2O |
| B、碳酸氢铵溶液中加入足量氢氧化钡溶液:NH4++HCO3-+2OH-═CO32-+NH3?H2O+H2O |
| C、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
| D、Ca(HCO3)2溶液中加入少量的NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
不能用来判断醋酸属于弱电解质的实验事实是( )
| A、向某浓度的醋酸钠溶液滴入几滴酚酞试液:溶液由无色变为浅红色 |
| B、向滴有甲基橙试液的醋酸溶液加入少量醋酸钠晶体:振荡后溶液由红色变为橙色 |
| C、通过对比不同浓度的导电实验:醋酸溶液的导电性较盐酸溶液的导电性弱 |
| D、取相同体积pH=1的盐酸和醋酸溶液,分别加入足量的锌,用排水法收集生成的氢气:相同条件下,醋酸生成的氢气体积大 |
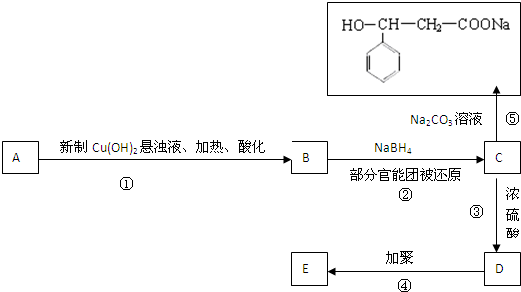
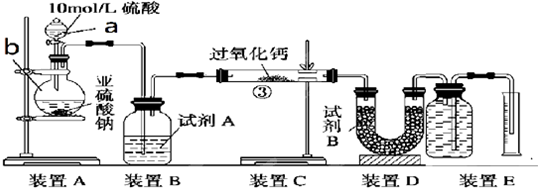
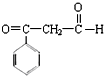 是一种重要的化工原料.A、B、C、D、E之间的转化关系如图:
是一种重要的化工原料.A、B、C、D、E之间的转化关系如图: