题目内容
20.在一定温度下,向体积恒定为2L的密闭容器里充入2mol M和一定量的N,发生如下 反应:M(g)+N(g)?E(g).当反应进行到4min时达到平衡,测得M的浓度为0.2mol•L-1.下列说法正确的是( )| A. | 4 min时,M的转化率为80% | |
| B. | 4 min时,用M表示的反应速率为0.8 mol•L-1•min-1 | |
| C. | 4 min后,向容器中充入不参与反应的稀有气体,M的物质的量减小 | |
| D. | 2 min时,M的物质的量浓度为0.6 mol•L-1 |
分析 A.M的转化率=$\frac{反应消耗浓度}{反应前总浓度}$×100%;
B.依据反应速率=$\frac{△c}{△t}$计算得到;
C.恒温恒容容器中加入惰气,总压增大,分压不变,平衡不动;
D.依据极值分析法,反应从开始到平衡的过程中,正反应速率越来越小,当进行2min时,M浓度的变化值大于0.4mol•L-1,所以2min时,M的物质的量浓度应小于0.6mol•L-1.
解答 解:A.反应开始时,M的浓度为:$\frac{2mol}{2L}$=1mol/L,平衡时为0.2mol•L-1,转化了0.8mol•L-1,M转化率为80%.故A正确;
B.4min时,用M表示的反应速率为:$\frac{0.8mol/L}{4min}$=0.2mol•L-1•min-1,故B错误;
C.恒温恒容下,充入不反应的稀有气体,各组分的浓度没有发生变化,所以正逆反应速率不变,平衡不移动,M的物质的量不变;故C错误;
D.反应从开始到平衡的过程中,正反应速率越来越小,当进行2min时,M浓度的变化值大于0.4mol•L-1,所以2min时,M的物质的量浓度应小于0.6mol•L-1,故D错误;
故选A.
点评 本题考查化学平衡的计算,题目难度中等,涉及反应速率、反应物的转化率、影响平衡条件分析判断,D为易错点,注意随着反应的进行,正反应速率逐渐减小,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
10.下表中对“2”的含义解释正确的一组是( )
| ${\;}_{1}^{2}$H | 2He | 2Cl | Ba2+ | |
| A | 质量数 | 中子数 | 质子数 | 电荷数 |
| B | 质量数 | 质子数 | 原子个数 | 电荷数 |
| C | 质子数 | 中子数 | 原子个数 | 电荷数 |
| D | 质量数 | 质子数 | 中子数 | 电荷数 |
| A. | A | B. | B | C. | C | D. | D |
8.下列说法正确的是( )
| A. | 汽油是纯净物 | |
| B. | 天然气是可再生能源 | |
| C. | 煤的干馏是化学变化 | |
| D. | 石油的分馏、裂化、裂解均是化学变化 |
15.分子式为C3H4Cl2且含有 结构的有机物的同分异构体共有(不考虑立体异构)( )
结构的有机物的同分异构体共有(不考虑立体异构)( )
 结构的有机物的同分异构体共有(不考虑立体异构)( )
结构的有机物的同分异构体共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
5.某课外实验小组设计的下列实验合理的是( )
| A. | 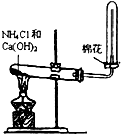 制备少量氨气 | B. | 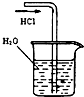 吸收HCl | ||
| C. |  分离苯和乙醇的混合物 | D. | 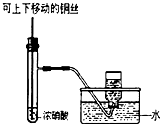 制备并收集少量NO2气体 |
12.25℃时,在①0.01mol/L的盐酸,②pH=2的醋酸,③pH=12的氨水,④0.01mol/L的NaOH溶液4种溶液中,由水电离出的c(H+)的大小关系是( )
| A. | ②>①>④>③ | B. | ①=②=③=④ | C. | ②=③>①=④ | D. | ②<①<③<④ |
9.钛是航空、军工、电力等领域的重要原料.工业上用钛酸亚铁(FeTiO3)冶炼钛(Ti)的过程是:
①2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2TiCl4+2FeCl3+6CO
②在氩气环境中,2Mg+TiCl4$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2
下列判断不正确的是( )
①2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2TiCl4+2FeCl3+6CO
②在氩气环境中,2Mg+TiCl4$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2
下列判断不正确的是( )
| A. | 反应②属于置换反应 | |
| B. | 反应②中氯化物的总质量保持不变 | |
| C. | 反应①、②中钛元素的化合价都改变 | |
| D. | 反应②中,氩气只作为保护气并不参加反应 |
8.能使甲基橙变红色的溶液中,一定能大量共存的离子组是( )
| A. | K+、Na+、HCO3-、Cl- | B. | K+、AlO2-、Br-、Cl- | ||
| C. | Na+、Cl-、NO3-、I- | D. | Al3+、NH4+、Cl-、SO42- |
 有A、B、C、D四种短周期元素,其中A元素和B元素的原子都有1个未成对电子,A+ 比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p 轨道中有3个未成对电子,其气态氢化物的水溶性在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4.请问答下列问题:
有A、B、C、D四种短周期元素,其中A元素和B元素的原子都有1个未成对电子,A+ 比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p 轨道中有3个未成对电子,其气态氢化物的水溶性在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4.请问答下列问题: ,CB3分子的VSEPR模型为四面体形.
,CB3分子的VSEPR模型为四面体形.