题目内容
下列说法正确的是( )
| A、反应热就是反应中放出的能量 |
| B、在101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
| C、由C(石墨)-→C(金刚石)△H=+1.9kJ/mol可知,金刚石比石墨稳定 |
| D、等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、在化学反应过程中放出或吸收的热量,通常叫反应热;
B、在101kPa时,1mol碳完全燃烧生成二氧化碳气体时所放出的热量碳的燃烧热;
C、石墨转化为金刚石属于吸热反应,说明等物质的量的石墨的能量低于金刚石的能量;
D、固体硫转化为蒸汽硫需要吸热.
B、在101kPa时,1mol碳完全燃烧生成二氧化碳气体时所放出的热量碳的燃烧热;
C、石墨转化为金刚石属于吸热反应,说明等物质的量的石墨的能量低于金刚石的能量;
D、固体硫转化为蒸汽硫需要吸热.
解答:
解:A、在化学反应过程中放出或吸收的热量,通常叫反应热,故A错误;
B、在101kPa时,1mol碳完全燃烧生成二氧化碳气体时所放出的热量碳的燃烧热,若不完全燃烧放出的热量就不是碳的燃烧热,故B错误;
C、石墨转化为金刚石属于吸热反应,说明等物质的量的石墨的能量低于金刚石的能量,因此石墨比金刚石稳定,故C错误;
D、蒸汽硫转化为固体硫需要放热,等量的硫蒸气和硫固体分别完全燃烧,产物相同,因此前者放出的热量多,故D正确;
故选D.
B、在101kPa时,1mol碳完全燃烧生成二氧化碳气体时所放出的热量碳的燃烧热,若不完全燃烧放出的热量就不是碳的燃烧热,故B错误;
C、石墨转化为金刚石属于吸热反应,说明等物质的量的石墨的能量低于金刚石的能量,因此石墨比金刚石稳定,故C错误;
D、蒸汽硫转化为固体硫需要放热,等量的硫蒸气和硫固体分别完全燃烧,产物相同,因此前者放出的热量多,故D正确;
故选D.
点评:本题考查了反应热的定义、分类和意义,题目难度不大,注意燃烧热的定义中要求生成稳定的氧化物.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
金属具有延展性的原因是( )
| A、金属原子半径都较大,价电子较少 |
| B、自由电子受外力作用时能迅速传递能量 |
| C、金属中大量自由电子受外力作用时,运动速度加快 |
| D、金属受外力作用变形时,金属阳离子与自由电子间仍保持较强烈作用 |
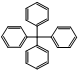 甲烷分子中的4个氢原子全部被苯基取代可得如图所示的分子,对该分子的描述正确的是( )
甲烷分子中的4个氢原子全部被苯基取代可得如图所示的分子,对该分子的描述正确的是( )| A、分子式为C25H18 |
| B、分子中所有原子有可能处于同一平面 |
| C、该化合物分子中所有原子不可能处于同一平面 |
| D、分子中所有原子一定处于同一平面 |
若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、1 mol Cl2作为氧化剂得到的电子数为2NA |
| B、14 g氮气中含有7NA个电子 |
| C、在0℃、101 kPa时,22.4 L氢气中含有NA个氢原子 |
| D、NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
下列溶液中有关物质的量浓度关系正确的是( )
| A、pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+)+c(M+)=c(OH-)一定成立 |
| B、0.2mol?L-1CH3COOH和0.1mol?L-1 NaOH等体积混合:c(CH3COO-)+2 c(OH-)=2c(H+)+c(CH3COOH) |
| C、pH 相等的CH3COONa、NaOH、Na2CO3三种溶液物质的量浓度为:c(NaOH)>c(CH3COONa)>c(Na2CO3) |
| D、0.1mol?L-1NaHA溶液,其pH=4,则c(HA-)>c(H+)>c(H2A)>c(A2-) |
“绿色化学”是21世纪化学发展的主导方向 之一,其核心是利用化学原理,从源头上减少或消除化学工业对环境的污染.据此判断,下列不属于“绿色化学”内容的是( )
| A、尽可能通过最小的成本取得最大的利润 |
| B、化工生产原料和产品尽可能无毒、无害或毒性极小 |
| C、反应在无毒、无公害的条件下进行,如采用无毒无害的溶剂和催化剂 |
| D、尽可能采用可再生原料,且原料的利用率尽可能最大化,副产品或废品尽可能最小化 |
1.92g铜与足量一定浓度的硝酸反应,铜恰好全部溶解,生成气体896mL(标准状况),整个过程消耗硝酸的物质的量是( )
| A、0.08mol |
| B、0.12mol |
| C、0.10mol |
| D、0.09mol |
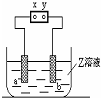 图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,a极板/b极板/X电极/Z溶液符合这一情况的是( )
图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,a极板/b极板/X电极/Z溶液符合这一情况的是( )| A、锌/石墨/负极/CuSO4 |
| B、石墨/石墨/负极/NaOH |
| C、银/铁/正极/AgNO3 |
| D、铜/石墨/负极/CuCl2 |
高分子化合物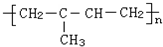 的单体是( )
的单体是( )
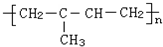 的单体是( )
的单体是( )| A、1,3-丁二烯 |
| B、2-甲基-1,3-丁二烯 |
| C、2-甲基-2-丁烯 |
| D、乙烯和丙烯 |