题目内容
8.下列物质的水溶液因水解而呈酸性的是( )| A. | NH4Cl | B. | Na2SO4 | C. | NaHCO3 | D. | Ba(NO3)2 |
分析 能水解的是含弱离子的盐,而强酸弱碱盐水解显酸性,强碱弱酸盐水解显碱性,强碱强酸盐不水解,据此分析.
解答 解:A、氯化铵是强酸弱碱盐,水解显酸性,故A正确;
B、硫酸钠是强酸强碱盐,不能水解,溶液显中性,故B错误;
C、碳酸氢钠是强碱弱酸的酸式盐,碳酸氢根既能水解又能电离,且水解程度大于电离程度,故溶液显碱性,故C错误;
D、硝酸钡是强酸强碱盐,不能水解,溶液显中性,故D错误.
故选A.
点评 本题考查了溶液显酸性的因素,应注意的是显酸性的溶液不一定是酸溶液,但酸溶液一定显酸性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.高铁酸钾(K2FeO4)是一种新型多功能水处理剂.其生产工艺的部分流程如下,下列说法正确的是( )


| A. | 在除去KCl的过程中必须用到过滤操作 | |
| B. | 在Cl2与KOH反应时,KOH作还原剂 | |
| C. | 在溶液A中加入KOH固体的作用是使KClO3转化为KClO | |
| D. | 在溶液A中加入KOH固体的作用是放出更多的热量,有利于提高反应速率 |
11.在盛放浓硝酸的试剂瓶中的标签上应印有下列警示标记中的( )
| A. |  | B. |  | C. |  | D. |  |
8.制备Al2Fe(SO4)4•24H2O的实验中,对过滤出产品的母液(pH<1)进行处理.常温下,分别取母液并向其中加入指定物质,反应后溶液中主要存在的一组离子正确的是( )
| A. | 通入足量氨气:NH4+、SO42-、OH-、AlO2- | |
| B. | 加入足量Na2O2:Na+、Fe2+、SO42-、OH- | |
| C. | 加入过量稀硝酸:Al3+、Fe3+、H+、NO3-、SO42- | |
| D. | 加入过量漂白粉溶液:Ca2+、Fe2+、Cl-、ClO- |
17.某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)?Z(g)+W(s);△H>0,下列叙述正确的是( )
| A. | 加入少量W,逆反应速率增大 | |
| B. | 当容器中气体压强不变时,一定是n(X):n(Y):n(Z)=1:1:1 | |
| C. | 当容器中气体的平均相对分子质量不变时,一定是V(X):V(Y):V(Z)=1:1:1 | |
| D. | 加入X,上述反应的△H增大 |
18.下列实验不能达到预期目的是( )
| 编号 | 实验内容 | 实验目的 |
| A | 配制100mL 1.0mol•L-1 CuSO4溶液 | 将25.0g CuSO4•5H2O溶于蒸馏水配成100mL溶液 |
| B | 测定混有Na2CO3的NaCl固体样品中NaCl的质量分数 | 取m1 g样品加入过量盐酸充分反应,加热蒸干后,称量固体质量为m2 g |
| C | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| D | 用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 验证氧化性:H2O2比Fe3+强 |
| A. | A | B. | B | C. | C | D. | D |
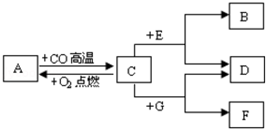 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为FeSO4溶液,G为CuSO4溶液,它们之间存在如图所示关系:
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为FeSO4溶液,G为CuSO4溶液,它们之间存在如图所示关系: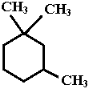 ,
,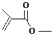 :
: .
.