题目内容
18.“类推”是学习化学的一种好方法.但是有些“类推”也会由于物质的特性等原因产生错误.下列几种类推结论中正确的是( )| A. | 金属镁能在CO2中燃烧,则金属钠也能在CO2中燃烧 | |
| B. | 金属钠与水反应产生NaOH和H2,则金属铜与水反应也能产生Cu(OH)2和H2 | |
| C. | Cl2+H2O?HCl+HClO是氧化还原反应,则ICl+H2O?HCl+HIO也是氧化原反应 | |
| D. | CO2与H2O反应生成H2CO3,则SiO2与H2O反应也可以生成H2SiO3 |
分析 A、金属钠的活泼性强于镁;
B、活泼金属可以和水反应生成碱和氢气,而铜不活泼金属不与水反应;
C、氧化还原反应一定有化合价的变化;
D、二氧化硅不溶于水,也不与水反应.
解答 解:A、金属钠的活泼性强于镁,也能在二氧化碳中燃烧生成过氧化钠和碳,故A正确;
B、活泼金属钠与水反应生成NaOH和H2,金属与水反应不一定生成碱,故B错误;
C、ICl+H2O═HCl+HIO中没有化合价的变化,不属于氧化还原反应,故C错误;
D、二氧化硅不溶于水,也不与水反应,所以硅酸不能由二氧化硅与水反应制得,故D错误;
故选A.
点评 本题考查了钠的性质、氧化还原反应、硅酸的制取,题目难度不大,熟悉钠与盐溶液反应,先与溶剂水反应,生成的碱再与溶质作用.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
9.下列说法不正确的是( )
| A. | 物质燃烧总是放热的 | |
| B. | 放热反应在反应发生时都不需要加热 | |
| C. | 热化学方程式中,化学式前的化学计量数仅表示物质的量 | |
| D. | 大多数化合反应是放热的,大多数分解反应是吸热的 |
6.下列说法正确的是( )
| A. | 有单质生成的分解反应一定是氧化还原反应 | |
| B. | 某元素从化合态变为游离态时,该元素一定被还原 | |
| C. | 氧化剂被氧化,还原剂被还原 | |
| D. | 没有氧元素参加的反应一定不是氧化还原反应 |
13.实验室制硝基苯,正确的操作是( )
| A. | 将苯和硝酸混和,再加入浓硫酸,冷却 | |
| B. | 先加苯,再加浓硫酸,最后加入浓硝酸 | |
| C. | 在浓硝酸中加入浓硫酸,冷却后加入苯 | |
| D. | 在浓硫酸中加入浓硝酸,冷却后加入苯 |
3.“类推”是一种重要的学习方法,但有时会产生错误结论,下列类推结论中正确的是( )
| A. | 碱金属氟化物的晶格能顺序是LiF>NaF>KF>RbF>CsF;则钠的卤化物的晶格能顺序是NaF>NaCl>NaBr>NaI | |
| B. | ⅣA族元素氢化物沸点顺序是GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序是AsH3>PH3>NH3 | |
| C. | 晶体中有阴离子,必有阳离子;则晶体中有阳离子,必有阴离子 | |
| D. | 若盐酸的浓度是醋酸浓度的2倍;则盐酸中H+浓度也是醋酸中H+浓度的2倍 |
10.在同温同压下,下列各组热化学方程式中,△H1>△H2的是( )
| A. | 2H2(气)+O2(气)═2H2O(气)△H1 2H2(气)+O2(气)═2H2O(液)△H2 | |
| B. | S(气)+O2(气)═SO2(气)△H1 S(固)+O2(气)═SO2(气)△H2 | |
| C. | C(固)+O2(气)═CO2(气)△H1 C(固)+$\frac{1}{2}$O2 (气)═CO(气)△H2 | |
| D. | H2(气)+Cl2(气)═2HCl(气)△H1 $\frac{1}{2}$H2(气)+$\frac{1}{2}$ Cl2(气)═HCl(气)△H2 |
7.如图中,表示正反应是放热反应的是( )
| A. | 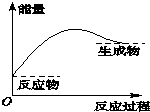 | B. | 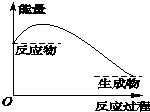 | C. | 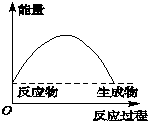 | D. | 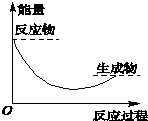 |
8.下列关于氧化还原反应的叙述中,正确的是( )
| A. | 有单质参加的反应一定是氧化还原反应 | |
| B. | 燃烧反应必须有氧气作氧化剂 | |
| C. | 2Fe+3Cl2═2FeCl3; Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS 由此可以判断氧化性:Cl2>S | |
| D. | Mg在化学反应中失去2个电子,而Al在化学反应中失去3个电子,因此还原性Al>Mg |