题目内容
4.下列说法正确的是( )| A. | 滴有酚酞的Na2CO3溶液中加入BaCl2溶液,红色褪去可证明BaCl2溶液显酸性 | |
| B. | 根据盐溶液的酸碱性,将盐分成酸式盐、正盐和碱式盐 | |
| C. | 泡沫灭火器是利用硫酸铝溶液和碳酸钠溶液反应产生大量CO2和Al(OH)3灭火 | |
| D. | NH4F溶液中含有少量的HF,因此NH4F溶液不能存放于玻璃试剂瓶中 |
分析 A.碳酸钠水解呈碱性,加入氯化钡沉淀碳酸钡沉淀,导致水解平衡向逆向移动,溶液碱性减弱;
B.依据盐的组成分类将盐分成酸式盐、正盐和碱式盐;
C.泡沫灭火器是利用硫酸铝溶液和碳酸氢钠溶液反应生成二氧化碳和Al(OH)3灭火;
D.NH4F溶液是弱酸弱碱盐,水解得到溶液中含HF,玻璃中的二氧化硅会和氢氟酸发生反应;
解答 解:A.Na2CO3为强碱弱酸盐,水解呈碱性,BaCl2与Na2CO3反应生成BaCO3沉淀,水解平衡逆向移动,溶液碱性减弱,故氯化钡是强酸强碱盐,溶液呈中性,A错误;
B.根据盐的组成,将盐分成酸式盐、正盐和碱式盐,酸式盐不一定显酸性,如NaHCO3溶液显碱性,NaHSO4显酸性,故B错误;
C.碳酸氢钠和硫酸铝发生双水解反应生成二氧化碳快,泡沫灭火器是利用硫酸铝溶液和碳酸氢钠溶液反应生成二氧化碳灭火,故C错误;
D.NH4F溶液是弱酸弱碱盐,水解得到溶液中含HF,NH4++F-+H2O?NH3•H2O+HF,生成的氢氟酸会和玻璃中的二氧化硅反应,因此NH4F溶液不能存放于玻璃试剂瓶中,故D正确;
故选D.
点评 本题考查了盐类水解原理分析,主要是影响水解平衡的因素、盐类水解的应用分析判断,题目难度中等.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
14.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | “84”消毒液中:K+、CO32-、Na+、I- | |
| B. | $\frac{K_W}{{C({H^+})}}$=1×10-13mol.L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | 能使PH试纸显蓝色的溶液中:Na+、CH3COO-、Fe3+、SO42- | |
| D. | 通入足量的H2S后的溶液中:Al3+、Cu2+、SO42-、Cl- |
12.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,46g NO2与N2O4的混合气体含有原子总数为3NA | |
| B. | 92g甲苯中含有碳碳双键数目为3 NA | |
| C. | 1 L 1 mol•L-1的Na2CO3溶液中含有CO32-的数目为NA | |
| D. | 标准状况下,2.24L Cl2与水反应转移的电子数目为0.1NA |
19.下列结论正确的是( )
| A. | S(g)+O2(g)═SO2(g)△H1;S(s)+O2(g)═SO2(g)△H2,则△H1<△H2 | |
| B. | C(石墨,s)=C(金刚石,s)△H=+1.9 kJ•mol-1,则金刚石比石墨稳定 | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ•mol-1,则含20 g NaOH的稀溶液与稀醋酸恰好完全反应,放出的热量为28.7 kJ | |
| D. | 2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则碳的燃烧热等于110.5 kJ•mol-1 |
16.下列实验操作、现象及由此得出的结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | 两者与盐酸反应的速率相同 |
| B | 将0.1mol•L-1Na2CO3溶液滴入BaCl2溶液至不再有沉淀产生,再滴加0.1mol•L-1Na2SO4溶液 | 有白色沉淀并保持不变 | BaCO3不能转化为BaSO4 |
| C | 向含有Fe2+的MgSO4溶液中,先加H2O2溶液,然后再调溶液的pH约为5 | 有红褐色沉淀生成 | Fe2+被H2O2氧化为Fe3+ |
| D | 将Kl和FeCl3溶液在试管中混合后,加入庚烷,振荡,静置 | 下层溶液显紫红色 | 生成的l2全部溶于庚烷中 |
| A. | A | B. | B | C. | C | D. | D |
13.下列化学用语表达正确的是( )
| A. | 乙烯的结构简式:C2H4 | B. | 甲烷分子的球棍模型: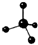 | ||
| C. | NaCl的电子式: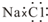 | D. | 氟离子的结构示意图: |
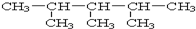 :2,3,4-三甲基戊烷.
:2,3,4-三甲基戊烷.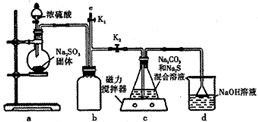 天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻污染.
天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻污染.