题目内容
下列离子在溶液中能大量共存的是( )
| A、Fe3+ NH4+ SCN- Cl- |
| B、Ba2+ H+ NO3- SO42- |
| C、Fe3+ Fe2+ Na+ NO3- |
| D、Fe2+ NH4+ Cl- OH- |
考点:离子共存问题
专题:
分析:如离子之间不发生反应生成沉淀、气体、弱电解质或不发生氧化还原反应、互促水解、络合等类型的反应,则离子能大量共存.
解答:
解:A.Fe3+、SCN-发生络合反应,不能大量共存,故A错误;
B.Ba2+、SO42-反应生成沉淀,不能大量共存,故B错误;
C.离子之间不发生任何反应,可大量共存,故C正确;
D.Fe2+、NH4+与OH-反应,不能大量共存,故D错误.
故选C.
B.Ba2+、SO42-反应生成沉淀,不能大量共存,故B错误;
C.离子之间不发生任何反应,可大量共存,故C正确;
D.Fe2+、NH4+与OH-反应,不能大量共存,故D错误.
故选C.
点评:本题考查离子共存,为高频考点,侧重学生的分析能力的考查,题目难度不大,解答本题注意常见离子的性质,判断离子之间能否发生反应.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
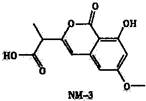 M-3是种正处于临床试验阶段的小分子抗癌药物,其结构如图所示(未表示出其空间构型).下列关于NM-3的性质描述正确的是( )
M-3是种正处于临床试验阶段的小分子抗癌药物,其结构如图所示(未表示出其空间构型).下列关于NM-3的性质描述正确的是( )| A、不含有手性碳原子 |
| B、能使溴的四氯化碳溶液褪色 |
| C、能与FeC13溶液发生显色反应 |
| D、1mo1该物质最多可与2mo1NaOH反应 |
在无色透明溶液中,能大量共存的离子组是( )
| A、Cu2+、Na+、SO42-、Cl- |
| B、K+、Na+、HCO3-、NO3- |
| C、OH-、HCO3-、Ca2+、Na+ |
| D、Ba2+、Na+、OH-、NO3- |
X、Y、Z、M、W为五种短周期元素.它们在周期表的相对位置如下表:则下列说法正确的是( )
| M | |||||||
| X | Y | Z | |||||
| W |
| A、Y、M形成的气态化合物在标准状况下的密度为0.76 g.L-1 |
| B、原子半径:W>Z>Y>X>M |
| C、由X元素形成的单质一定是原子晶体 |
| D、XZ2、X2M2、W2Z2均为直线型的共价化合物 |
已知氢气中1mol H-H断裂时吸收热量为436kJ,且氧气中1mol O=O键完全断裂时吸收热量496kJ,水蒸气中1mol H-O键形成时放出热量463kJ,则1mol氢气完全燃烧生成水蒸气时放出热量( )
| A、221 kJ |
| B、557 kJ |
| C、242 kJ |
| D、188 kJ |
 食醋分为酿造醋和配制醋两种.国家标准规定酿造食醋总酸含量不得低于3.5g/100mL.
食醋分为酿造醋和配制醋两种.国家标准规定酿造食醋总酸含量不得低于3.5g/100mL.