题目内容
14.下列不能说明硫的非金属性比氯的非金属性弱的是( )| A. | 硫酸比次氯酸稳定 | B. | 硫酸的酸性弱于高氯酸 | ||
| C. | H2S比HCl被氧化 | D. | 气态HC1比气态H2S稳定 |
分析 比较非金属元素的非金属性强弱,可根据单质之间的置换反应、对应最高价氧化物的水化物的酸性、氢化物的稳定性等角度判断.
解答 解:A.不能根据含氧酸的稳定性判断的非金属性的强弱,故A错误;
B.元素的非金属性越强,对应最高价氧化物的水化物的酸性越强,HClO4酸性比H2SO4强,可说明氯元素的非金属性比硫元素强,故B正确;
C.不能根据H2S比HCl易被氧化比较非金属性,例如H2S比HCl被氧化易被氧化,但非金属性Cl>S,故C错误;
D.元素的非金属性越强,对应氢化物的稳定性越强,氯化氢比硫化氢稳定,可说明氯元素的非金属性比硫元素强,故D正确;
故选AC.
点评 本题考查非金属性的判断,题目难度不大,注意非金属性的递变规律以及比较非金属性的角度.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
4.O2和O3是氧元素的两种结构不同的单质,1mol O2转化为O3时要吸收94.73kJ的热能.下列说法正确的是( )
| A. | O3比O2稳定 | |
| B. | O2和O3是氧的两种核素,互称同素异形体 | |
| C. | O2和O3的相互转化是化学变化 | |
| D. | 在标准状况下,等体积的O2和O3含有相同数目的氧原子 |
5.一定条件下的可逆反应2NO2 (红棕色)?2NO (无色)+O2 (无色),在恒压密闭容器充入NO2,达到化学平衡状态的标志是( )
| A. | 反应停止了 | |
| B. | NO的正反应速率与O2的逆反应速率相等 | |
| C. | c(NO):c(O2)=2:1 | |
| D. | 气体的颜色不再变化 |
2.下列关于晶体的说法,不正确的是( )
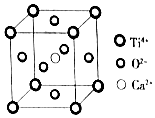
( Ti4+位于顶点上,O2-位于面心上,Ca2+位于中心)

( Ti4+位于顶点上,O2-位于面心上,Ca2+位于中心)
| A. | 该晶体的化学式为CaTiO3 | |
| B. | 该晶体中每个Ti4+和8个O2-相紧邻 | |
| C. | 一个CO2晶胞中平均含有4个CO2分子 | |
| D. | 金属晶体的熔点可能比分子晶体的熔点低 |
9.下列关于元素周期律和元素周期表的论述中正确的是( )
| A. | 同一主族的元素从上到下金属性逐渐减弱 | |
| B. | 元素周期表是元素周期律的具体表现形式 | |
| C. | 同一周期从左到右,元素原子半径逐渐增大 | |
| D. | 非金属元素的最高正化合价等于它的负化合价的绝对值 |
19.某同学设计如下三个实验方案以探究某反应是放热反应还是吸热反应:
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10mL 2mol•L-1稀硫酸,再插入一支温度计,温度计的温度由20℃逐渐升至35℃,随后,温度逐渐下降至30℃,最终停留在20℃.
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10mL 2mol•L-1硫酸溶液,再向其中加入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来.
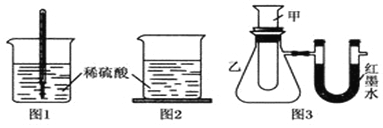
方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红墨水液面高低判断某反应是吸热反应还是放热反应.
根据上述实验回答相关问题:
(1)方案一中,温度先升高的原因是铝和硫酸反应放出的热量使烧杯里溶液的温度升高,
升至最大值后又逐渐下降的原因是反应完全后,热量向空气中传递,烧杯里物质的温度降低.
(2)方案二中,小木片脱落的原因是氢氧化钠与硫酸的反应放热.
(3)由方案三的现象得出结论:①③④组物质发生的反应都是放热(填“吸热”或“放热”)反应.
(4)方案三实验②的U形管中的现象为红墨水液面左高右低,说明反应物的总能量小于(填“大于”“小于”或“等于”)生成物的总能量.
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10mL 2mol•L-1稀硫酸,再插入一支温度计,温度计的温度由20℃逐渐升至35℃,随后,温度逐渐下降至30℃,最终停留在20℃.
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10mL 2mol•L-1硫酸溶液,再向其中加入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来.

方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红墨水液面高低判断某反应是吸热反应还是放热反应.
| 序号 | 甲试管里发生反应的物质 | U形管里红墨水液面 |
| ① | 氧化钙与水 | 左低右高 |
| ② | 氢氧化钡晶体与氯化铵晶体(充分搅拌) | ? |
| ③ | 铝片与烧碱溶液 | 左低右高 |
| ④ | 铜与浓硝酸 | 左低右高 |
(1)方案一中,温度先升高的原因是铝和硫酸反应放出的热量使烧杯里溶液的温度升高,
升至最大值后又逐渐下降的原因是反应完全后,热量向空气中传递,烧杯里物质的温度降低.
(2)方案二中,小木片脱落的原因是氢氧化钠与硫酸的反应放热.
(3)由方案三的现象得出结论:①③④组物质发生的反应都是放热(填“吸热”或“放热”)反应.
(4)方案三实验②的U形管中的现象为红墨水液面左高右低,说明反应物的总能量小于(填“大于”“小于”或“等于”)生成物的总能量.
6.下列各组离子在指定条件下可能大量共存的是( )
| A. | 不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、ClO- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、NH4+ | |
| C. | 常温下水电离出的c(H+ )•c(OH- )=10-20的溶液中:Na+、Cl-、S2-、SO32- | |
| D. | 无色透明溶液:K+、HCO3-、NO3-、SO42-、Fe3+ |
7.某研究小组经查阅资料得知:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO3↑+SO2↑;FeSO4$\frac{\underline{\;高温\;}}{\;}$FeO+SO3↑,SO3的熔点是16.8℃,沸点是44.8℃.
I.该小组探究在酒精喷灯加热条件下FeSO4分解的气体产物,实验装置如图所示.
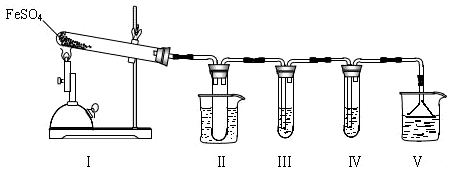
(1)装置Ⅱ的试管中不装任何试剂,其作用是防止溶液倒吸入装置Ⅰ中(或安全瓶),试管浸泡在50℃的水浴中,目的是防止SO3液化或凝固.
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验气体产物成分.请完成实验设计,填写检验试剂、预期现象与结论.
限选试剂:3mol•L-1 H2SO4溶液、6mol•L-1 NaOH溶液、0.5mol•L-1 BaCl2溶液、0.5mol•L-1 Ba(NO3)2溶液、0.01mol•L-1酸性KMnO4溶液、0.01mol•L-1溴水.
Ⅱ.FeSO4固体往往含有Fe2(SO4)3杂质,该研究小组采用称重法确定固体中铁元素的质量分数,操作流程为:

请根据流程回答:
(1)操作Ⅱ中必须用到的仪器是A
A.25mL酸式滴定管 B.50mL 量筒 C.25mL 量筒 D.25mL碱式滴定管
(2)系列操作名称依次为过滤、洗涤、灼烧.
(3)若最终测得红棕色固体质量为3.2g,则样品中铁元素的质量分数为70%.
I.该小组探究在酒精喷灯加热条件下FeSO4分解的气体产物,实验装置如图所示.

(1)装置Ⅱ的试管中不装任何试剂,其作用是防止溶液倒吸入装置Ⅰ中(或安全瓶),试管浸泡在50℃的水浴中,目的是防止SO3液化或凝固.
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验气体产物成分.请完成实验设计,填写检验试剂、预期现象与结论.
限选试剂:3mol•L-1 H2SO4溶液、6mol•L-1 NaOH溶液、0.5mol•L-1 BaCl2溶液、0.5mol•L-1 Ba(NO3)2溶液、0.01mol•L-1酸性KMnO4溶液、0.01mol•L-1溴水.
| 检验试剂 | 预期现象和结论 |
| 装置Ⅲ的试管中加入0.5 mol•L -1 BaCl2. | 产生大量白色沉淀,证明气体产物中含有SO3. |
| 装置Ⅳ的试管中加入0.01 mol•L-1 酸性 KMnO4 溶液(或0.0l mol•L-1 溴水). | 若溶液紫色(或橙色)褪去,证明气体产物中含有SO2,若溶液紫色(或橙色)无明显变化,证明气体产物中不含SO2 |

请根据流程回答:
(1)操作Ⅱ中必须用到的仪器是A
A.25mL酸式滴定管 B.50mL 量筒 C.25mL 量筒 D.25mL碱式滴定管
(2)系列操作名称依次为过滤、洗涤、灼烧.
(3)若最终测得红棕色固体质量为3.2g,则样品中铁元素的质量分数为70%.