题目内容
13.下列物质的水溶液因水解而呈碱性的是( )| A. | KOH | B. | Na2CO3 | C. | AlCl3 | D. | CaO |
分析 水溶液因水解而呈碱性,说明该盐为强碱弱酸盐,据此进行解答.
解答 解:A.KOH为强碱,在溶液不不能水解,故A错误;
B.Na2CO3为强碱弱酸盐,碳酸根离子部分水解,溶液呈碱性,故B正确;
C.AlCl3为强酸弱碱盐,其溶液呈酸性,故C错误;
D.CaO是碱性氧化物,与水反应生成碱,不发生水解,故D错误;
故选B.
点评 本题考查了盐的水解原理,题目难度不大,明确盐的水解原理为解答关键,注意掌握常见盐的类型与溶液酸碱性的关系,试题培养了学生的灵活应用能力.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
3.100℃时,向容积为2L的密闭容器中充入一定量的X气体和Y气体,发生如下反应:X(g)+2Y(g)?Z(g)反应过程中测定的部分数据见表:
下列说法正确的是( )
| 反应时间/min | n(X)/mol | n(Y)/mol |
| 0 | 2.00 | 2.40 |
| 10 | 1.00 | |
| 30 | 0.40 |
| A. | 前10 min内反应的平均速率为v(Z)=0.10 mol•L-1•min-1 | |
| B. | 温度为200℃时,上述反应平衡常数为20,则正反应为吸热反应 | |
| C. | 若密闭容器体积可变,其他条件不变,在达到平衡后缩小容器体积为原来一半,则c(X)<1mol/L | |
| D. | 保持其他条件不变,向容器中再充入1.00 mol X气体和1.20 mol Y气体,到达平衡后,X转化率增大 |
4.某化合物的化学式为NH5,其电子式为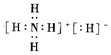 下列有关说法正确的是( )
下列有关说法正确的是( )
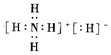 下列有关说法正确的是( )
下列有关说法正确的是( )| A. | 该化合物中氢元素的化合价均为+1价 | |
| B. | 该化合物中只有N原子最外层达到稀有气体的稳定结构 | |
| C. | 该化合物中含有$\stackrel{-1}{H}$与$\stackrel{+1}{H}$,二者互为同位素 | |
| D. | 该化合物中既含有共价键,又含有离子键 |
1.下列关于有机物的叙述正确的是( )
| A. | 聚乙烯塑料中含有大量碳碳双键,容易老化 | |
| B. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| C. | 甲苯苯环上的一个氢原子被一C3H6Cl取代,形成的同分异构体有9种 | |
| D. | CH2═CHCH2OH能发生加成反应、取代反应、氧化反应 |
8. 常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示.反应过程中有红棕色气体产生.下列说法错误的是( )
常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示.反应过程中有红棕色气体产生.下列说法错误的是( )
 常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示.反应过程中有红棕色气体产生.下列说法错误的是( )
常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示.反应过程中有红棕色气体产生.下列说法错误的是( )| A. | t1时刻前,A1片的电极反应为:2A1-6e-+3H2O═A12O3+6H+ | |
| B. | t1时,因A1在浓硝酸中钝化,氧化膜阻碍了A1继续反应 | |
| C. | t1之后,负极Cu失电子,电流方向发生改变 | |
| D. | 烧杯中发生的离子反应为:2NO2+2OH-═2NO3-+H2O |
18.下列试剂中,可以鉴别二氧化碳和二氧化硫的是( )
| A. | 澄清石灰水 | B. | 品红溶液 | ||
| C. | 湿润的蓝色石蕊试纸 | D. | 硝酸银溶液 |
4.醋酸在水中电离方程式可表示为:CH3COOH?CH3COO-+H+△H>0,下列操作能使H+浓度增大的是( )
| A. | 加入少量NaOH固体 | B. | 加热升温10℃ | ||
| C. | 加入锌粉 | D. | 加入固体CH3COONa |
1.下列所得溶液的物质的量浓度等于0.1mol•L-1的是( )
| A. | 将0.1 mol HCl充分溶解在1 L水中 | |
| B. | 将60 g质量分数为10%的醋酸与940 g水混合 | |
| C. | 将3.1 g氧化钠溶于水并配成1 L溶液 | |
| D. | 将14.2 g Na2SO4•10H2O溶于水中配成1 L溶液 |
2.为了提纯表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 甲烷(乙烯) | 酸性KMnO4溶液 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | 苯(甲苯) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | 溴水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |