题目内容
14.某温度下,2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+mY(g)?3Z(g)平衡时X、Y、Z的体积分数分别为30%、60%、10%.在此平衡体系中又加入1molZ(g),再达平衡后,X、Y、Z的体积分数不变.下列不正确的是( )| A. | m=2 | |
| B. | 第二次平衡时,Z的浓度为0.2mol•L-1 | |
| C. | 两次平衡的平衡常数相同 | |
| D. | 又加入1molZ,平衡没有发生移动 |
分析 A.在此平衡体系中加入1molZ(g),则可等效为两等效平衡体系合,在合并瞬间X、Y、Z的体积分数不变,但单位体积内体系分子总数增多,依据勒夏特列原理平衡应朝使单位体积内分子总数减小方向移动,但再次达到平衡后,X、Y、Z的体积分数不变,则说明m+1=3;
B.根据平衡时Z的体积分数计算出Z的物质的量,然后根据c=$\frac{n}{V}$计算出Z的浓度;
C.平衡常数不受浓度的影响,温度不变,平衡常数不变;
D.加入Z后平衡向着逆向移动.
解答 解:A.某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)?3Z(g),平衡时X、Y、Z的体积分数分别为30%、60%、10%,在此平衡体系中加入1molZ(g),则可等效为两等效平衡体系合,在合并瞬间X、Y、Z的体积分数不变,但单位体积内体系分子总数增多,依据勒夏特列原理平衡应朝使单位体积内分子总数减小方向移动,但再次达到平衡后,X、Y、Z的体积分数不变,则说明m+1=3,故m=2,故A正确;
B.m=2,则该反应为反应前后气体总量不变的反应,故第二次平衡时Z的物质的量为:4×10%=0.4mol,故Z的浓度为:$\frac{0.4mol}{2L}$=0.2mol/L,故B正确;
C.同一化学反应的平衡常数只与温度有关,两次平衡温度不变,故两次平衡的平衡常数相同,故C正确;
D.又加入1molZ,平衡发生移动,向着逆向移动,之至达到新的平衡,故D错误;
故选D.
点评 本题考查了化学平衡的影响因素,题目难度中等,根据题干数据正确判断m的值为解答关键,注意掌握影响化学平衡的因素,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
4.图是石油分馏塔的示意图,a、b、c三种馏分中( )
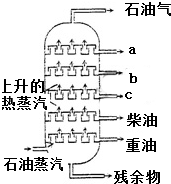

| A. | a的沸点最高 | B. | b的熔点最低 | ||
| C. | c的碳原子数最多 | D. | 每一种馏分都是纯净物 |
2.反应A+B═C,在反应过程中,断裂1mol A中的化学键消耗的能量为Q1kJ,断裂1mol B中的化学键消耗的能量为Q2kJ,形成1mol C中的化学键释放的能量为Q3kJ;1mol A所含化学能为E1kJ,1mol B所含化学能E2kJ,1molC 所含化学能E3kJ.下列说法中一定正确的是( )
| A. | 若Q1+Q2<Q3,则反应为放热反应 | B. | 若Q1+Q2>Q3,则反应为放热反应 | ||
| C. | 若E1+E2>E3,则反应为吸热反应 | D. | 若E1+E2>E3,则Q1+Q2>Q3 |
9.下列关于0.10mol•L-1NaHCO3溶液的说法正确的是( )
| A. | 温度升高,c(HCO3-)减小 | |
| B. | 25℃时,加水稀释后,n(H+)与n(OH-)的乘积变小 | |
| C. | 溶质的电离方程式为NaHCO3═Na++H++CO32- | |
| D. | 离子浓度关系:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) |
19.有①NaOH溶液②CH3COONa溶液各25mL,物质的量浓度均为0.1mol•L-1,下列说法正确的是( )
| A. | 两种溶液pH的大小顺序是②>① | |
| B. | 若将两种溶液稀释相同倍数,pH变化较大的是② | |
| C. | 若分别加入25mL0.1mol•L-1盐酸后,pH较大的是① | |
| D. | 若两种溶液的pH均为9,则物质的量浓度大小关系是①>② |
6.《三国志•诸葛亮传》记载了蜀汉丞相孔明南征孟获的战争中,蜀军误喝哑泉中毒,后经当地一老叟指点,蜀军喝了当地的安乐泉便脱离了危险,当代化学工作者对哑泉进行了考察,发现哑泉含有硫酸铜,安乐泉味苦,呈碱性,下列说法中不正确的是( )
| A. | 硫酸铜有毒 | B. | 硫酸铜溶液是蓝色的胶体 | ||
| C. | 硫酸铜为电解质 | D. | 解毒的原因是Cu2+转化为沉淀 |
3.ClO2是新一代饮用水的消毒剂,许多发达国家的自来水厂采用ClO2代替Cl2来进行自来水消毒.我国最近成功研制出制取ClO2的新方法,其反应的微观过程如下所示:
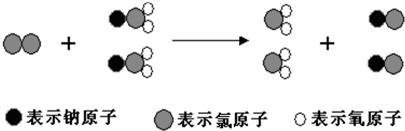
下列有关该反应的叙述中正确的是( )

下列有关该反应的叙述中正确的是( )
| A. | 该反应的化学方程式为Cl2+2NaClO2═2ClO2+2NaCl | |
| B. | 该反应是应是复分解反应 | |
| C. | 反应中Cl2既是氧化剂,又是还原剂 | |
| D. | NaClO2和ClO2中Cl元素的化合价相同 |
4.铜与稀硝酸反应,不能生成的物质是( )
| A. | Cu(NO3)2 | B. | NO | C. | H2O | D. | H2 |
 ;取代反应
;取代反应 ;加成反应
;加成反应 ;取代反应
;取代反应