题目内容
20.Na与H2O反应现象明显,下列现象中不符合事实的是( )| A. | 滴加了酚酞的溶液变红色 | B. | 产生气体推动Na游动 | ||
| C. | Na沉在水下 | D. | Na熔成光亮小球 |
分析 钠与水反应时产生的各种现象如下:钠浮在水面,然后熔化成闪亮黄色小球,在水面游动,并发出嘶嘶的响声.现象是物质性质的体现,根据钠的性质分析现象原因.
解答 解:A.钠与水反应生成氢氧化钠溶液为强碱溶液,滴加了酚酞的溶液变红色,故A正确;
B.钠和水反应生成氢气,由于受力不均导致钠在水面上四处游动,故B正确;
C.钠的密度小于水的密度,所以钠会浮在水面上,故C错误;
D.钠的熔点较低,钠与水反应放热使溶液温度升高,所以钠很快融化成为小球,故D正确;
故选C.
点评 本题考查了钠与水的反应.应从钠的强还原性和钠的物理性质来理解钠与水反应的现象,题目难度不大.

练习册系列答案
相关题目
10.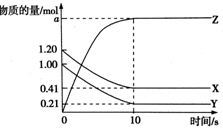 已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )
已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )
 已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )
已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )| A. | a为1.60 | |
| B. | X和Y的转化率相等 | |
| C. | 0~10min的平均速率V(Z)=0.079mol•L-1•min-1 | |
| D. | 容器内Z的浓度最大可以达到1.00 mol/L |
8.柠橡烯是一种食用香料,其结构为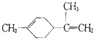 ; 有关柠檬烯的分析正确的是( )
; 有关柠檬烯的分析正确的是( )
 ; 有关柠檬烯的分析正确的是( )
; 有关柠檬烯的分析正确的是( )| A. | 柠檬烯的一氯代物有9种 | |
| B. | 柠檬烯和丁基苯 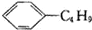 互为同分异构体 互为同分异构体 | |
| C. | 柠檬烯的分子中所有的碳原子可能在同一个平面上 | |
| D. | -定条件下,柠檬烯可以发生取代反应和氧化反应 |
5.50℃时的KCl饱和溶液,降低10℃,下列因素不发生变化的是( )
| A. | 溶解度 | B. | 溶质的质量分数 | C. | 溶剂的质量 | D. | 溶液的质量 |
9.由A、B、C、D四种金属按下表中装置进行实验.
根据实验现象回答下列问题:
①装置乙中正极的电极反应式是Cu2++2e-═Cu.
②四种金属活动性由强到弱的顺序是D>A>B>C.
| 装置 | 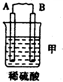 | 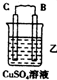 | 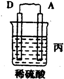 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置乙中正极的电极反应式是Cu2++2e-═Cu.
②四种金属活动性由强到弱的顺序是D>A>B>C.
4.实验小组以二氧化锰和浓盐酸为反应物,连接装置A→B→C制取氯水,并探究氯气和水反应的产物.
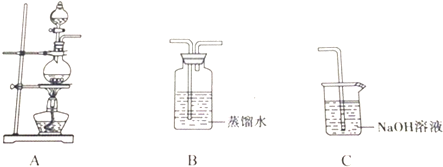
(1)A中发生反应的离子方程式是MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)B中得到浅黄绿色的饱和氯水,将所得氯水分三等份,进行的操作、现象、结论如下:
①甲同学指出:由实验Ⅰ得出的结论不合理,原因是制取的氯水中含有杂质HCl(填化学式),也能与碳酸氢钠反应产生气泡.应在A、B间连接除杂装置,请画出除杂装置并标出气体流向和药品名称.
②乙同学指出由实验Ⅱ得出的结论不合理,原因是实验未证明Cl2(填化学式)是否有漂白性.
③丙同学利用正确的实验装置发现氯水中有Cl-存在,证明氯水中有Cl-的操作和现象是:取少量氯水于试管中,加入硝酸银和稀硝酸,若有白色沉淀产生,说明有Cl-存在.丙同学认为,依据上述现象和守恒规律,能推测出氯水中有次氯酸存在.这一推测是否正确,请说明理由不正确,从实验可知,氯水中含H+、Cl-,即氯气与水反应生成了H+和Cl-,氯的化合价从零价降低到-1价,必然要有元素化合价升高,H已是最高价,不再升高,一定有其他元素化合价的升高,而氯元素不一定只升高到+1价.
④丁同学利用正确的实验装置和操作进行实验,观察到实验现象与实验Ⅰ、Ⅱ相似,说明氯气和水反应的产物具有的性质是酸性和漂白性.
(3)戊同学将第三份氯水分成两等份,向其中一份加入等体积的蒸馏水,溶液接近无色.另一份中加入等体积饱和的氯化钠溶液,溶液为浅黄绿色.对比这两个实验现象能说明:加入蒸馏水溶液接近无色,说明c(Cl2)几乎降低为零,加入等体积的饱和氯化钠溶液,溶液还是浅黄绿色,说明氯离子的加入又生成了Cl2,即氯气和水的反应是可逆反应,增大氯离子浓度,平衡向反应物方向移动,使Cl2增多,所以呈现浅绿色.

(1)A中发生反应的离子方程式是MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)B中得到浅黄绿色的饱和氯水,将所得氯水分三等份,进行的操作、现象、结论如下:
| 实验 | 实验操作 | 现象 | 结论 |
| Ⅰ | 向氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应至少产生了一种酸性强于碳酸的物质 |
| Ⅱ | 向品红溶液中滴入氯水 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
②乙同学指出由实验Ⅱ得出的结论不合理,原因是实验未证明Cl2(填化学式)是否有漂白性.
③丙同学利用正确的实验装置发现氯水中有Cl-存在,证明氯水中有Cl-的操作和现象是:取少量氯水于试管中,加入硝酸银和稀硝酸,若有白色沉淀产生,说明有Cl-存在.丙同学认为,依据上述现象和守恒规律,能推测出氯水中有次氯酸存在.这一推测是否正确,请说明理由不正确,从实验可知,氯水中含H+、Cl-,即氯气与水反应生成了H+和Cl-,氯的化合价从零价降低到-1价,必然要有元素化合价升高,H已是最高价,不再升高,一定有其他元素化合价的升高,而氯元素不一定只升高到+1价.
④丁同学利用正确的实验装置和操作进行实验,观察到实验现象与实验Ⅰ、Ⅱ相似,说明氯气和水反应的产物具有的性质是酸性和漂白性.
(3)戊同学将第三份氯水分成两等份,向其中一份加入等体积的蒸馏水,溶液接近无色.另一份中加入等体积饱和的氯化钠溶液,溶液为浅黄绿色.对比这两个实验现象能说明:加入蒸馏水溶液接近无色,说明c(Cl2)几乎降低为零,加入等体积的饱和氯化钠溶液,溶液还是浅黄绿色,说明氯离子的加入又生成了Cl2,即氯气和水的反应是可逆反应,增大氯离子浓度,平衡向反应物方向移动,使Cl2增多,所以呈现浅绿色.
 ;若XY2为共价化合物时,其结构式为:S=C=S.
;若XY2为共价化合物时,其结构式为:S=C=S.