题目内容
9.吸热反应一定是( )| A. | 释放能量 | |
| B. | 储存能量 | |
| C. | 反应物的总能量低于生成物的总能量 | |
| D. | 反应物的总能量高于生成物的总能量 |
分析 反应物的总能量低于生成物的总能量,反应是吸热反应,反应物的总能量高于生成物的总能量,反应是放热反应,据此回答.
解答 解:反应物的总能量低于生成物的总能量,反应是吸热反应,反应物的总能量高于生成物的总能量,反应是放热反应,吸热反应一定是储存能量的过程.
故选BC.
点评 本题考查化学反应中物质具有的能量与化学反应的热效应间的关系,难度不大,需正确理解放热、吸热的本质是解题的关键.

练习册系列答案
相关题目
6.下列叙述不正确的是( )
| A. | 甲烷和苯都能发生取代反应 | |
| B. | 甲烷和乙烯通常都是气体,可用溴水进行鉴别 | |
| C. | 甲烷和苯都无还原性,乙烯有还原性 | |
| D. | 乙烯和苯都能与氢气发生加成反应,反应产物都属于烃 |
20.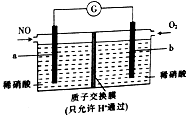 用NO生产硝酸,可以有效消除污染,其原理如图所示.下列说法正确的是( )
用NO生产硝酸,可以有效消除污染,其原理如图所示.下列说法正确的是( )
 用NO生产硝酸,可以有效消除污染,其原理如图所示.下列说法正确的是( )
用NO生产硝酸,可以有效消除污染,其原理如图所示.下列说法正确的是( )| A. | a极是该电极的正极 | |
| B. | 电流由a极经导线流向b极 | |
| C. | a极的电极反应式为NO-3e-+2H2O═NO3-+4H+ | |
| D. | 若消耗2.24L(标准状况下)氧气,则会有0.4 molH+通过质子交换膜进入a极区 |
4.近期“五水共治”越来越引起人们的重视,已知可以通过微电池除去废水中的乙酸钠和对氯苯酚其原理如图所示,下列说法正确的是( )
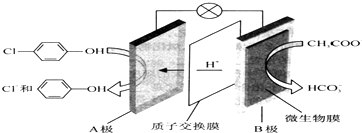

| A. | B为电池的正极,发生还原反应 | |
| B. | A极的电极反应式为: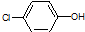 +e-=Cl-+ +e-=Cl-+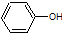 | |
| C. | 电流方向为从B极沿导线经小灯泡流向A极 | |
| D. | 当外电路中有0.2mole-转移时,通过质子交换膜的H+个数为0.2NA |
14.下列说法正确的是( )
| A. | 100℃时水的离子积常数Kw为5.5×10-13,说明水的电离是放热反应 | |
| B. | 配制Fe(NO3)2溶液时,为了防止Fe2+水解可向溶液中加入适量的稀硝酸 | |
| C. | NaClO溶液中通入少量CO2,ClO-水解程度增大,溶液碱性增强 | |
| D. | 0.1 mol/L CH3COOH溶液加水稀释后,CH3COOH的电离程度和溶液中c(OH-)都增大 |
1.二甲苯与苯类似,都能与H2发生加成反应.1,2二甲苯(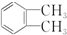 )加氢产物1,2二甲基环己烷(
)加氢产物1,2二甲基环己烷( )的一氯代产物有(不考虑立体异构)( )
)的一氯代产物有(不考虑立体异构)( )
 )加氢产物1,2二甲基环己烷(
)加氢产物1,2二甲基环己烷( )的一氯代产物有(不考虑立体异构)( )
)的一氯代产物有(不考虑立体异构)( )| A. | 5种 | B. | 6种 | C. | 3种 | D. | 4种 |
19.pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10-3mol•L-1,则该溶液中溶质的pC=3.下列说法正确的是( )
| A. | 某温度下,任何电解质的水溶液中:pC(H+)+pC(OH-)=14 | |
| B. | 某温度下,AB难溶性离子化合物的Ksp=1.0×10-10,其饱和溶液中:pC(A+)+pC(B-)=10 | |
| C. | 0.01mol/L的盐酸滴定某浓度的氨水溶液,滴定终时:pC(Cl-)>pC(NH4+)>pC(H+)>pC(OH-) | |
| D. | 0.01mol/L的醋酸钠溶液中:pC(Na+)+pC(H+)=pC(OH)-+pC(CH3COO-) |
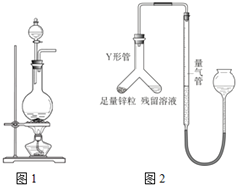 实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图所示).
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图所示).